از دست رفتن زودرس حاملگی
Early Pregnancy Loss
اصطلاح سقط (abortion) که در برخی از بیماران اثر منفی دارد، بتدریج توسط لغت miscarriage در حال جایگزینی است. هر دو اصطلاح در اصل مؤید دفع محصولات حاملگی قبل از هفته ی بیستم بارداری هستند، اما پزشکان عموماً جهت توصیف دفع محصولات حاملگی در سه ماهه اول از این اصطلاحات استفاده می کنند. این محدوده های زمانی توافقی بعلت پیشرفت در سونوگرافی تشخیصی و بیولوژی تکاملی کمتر مودر استفاده قرار می گیرند. دوره ی پیش رویانی (Preembryonic) از اولین روز آخرین سیکل قاعدگی تا 5 هفته بعد از آن است. دوره ی رویانی (embryonic) از هفته ی 6 بارداری تا هفته 9 بوده، دوره جنینی (fetal) از 10 هفتگی تا زمان زایمان را شامل می شود.
اپیدمیولوژی
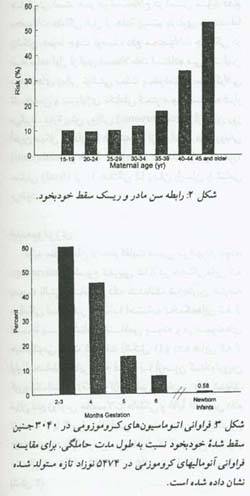
تولید مثل انسان از عدم کفایت نسبی برخوردار بوده، miscarriage با شیوع تقریبی 15% در حاملگی هایی که به صورت بالینی تشخیص داده شده اند، شایعترین عارضه حاملگی است. هر چند، با احتساب تخمک هایی یکه از لحاظ بافت شناسی ناقص بوده ودر نمونه های هیسترکتومی یافت شده اند و داده هایی که از اوایل حاملگی هایی که فقط با آزمون گنادوتروپین کوریونیک انسانی (hCG-?) حساس تشخیص داده شده اند، میزان رفع زودرس محصولات حاملگی و غالباً تشخیص داده نشده به 2 یا 3 برابر افزایش می یابد. هم چنین شیوع miscarriage با بالا رفتن سن مادر از 12% در زنان جوانتر از 20 سال تا 50% در زنان بالای 45 سال، افزایش می یابد.
اتیولوژی
در حضور رخدادهای پیچیده ژنتیکی، هورمونی، ایمونولوژی و سلولی که برای لقاح و لانه گزینی نیاز به هماهنگی و اجماع دقیق دارند، قابل توجه است که حاملگیهای موفقیت آمیز به کرات صورت می گیرند. دفع زودرس محصولات حاملگی می تواند به علل عوامل رویانی وپره ناتال باشد.
عوامل رویانی
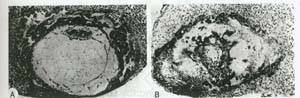
اکثر دفع های منفرد اسپورادیک بعلل ناقص داخلی غیرتکرار در مراحل نمو محصولات حاملگی، مانند ژرم سل های غیرطبیعی، جایگزینی ناقص، اشکال در تکامل رویان یا جفت، صدمات اتفاقی به جنین و یا دیگر علل ناشناخته رخ می دهند. پنجاه درصد از زنانی که با لکه بینی و کرامپ مراجعه می کنند، در سونوگرام دارای یک محصول حاملگی غیرزنده هستند، و تعدادی از این رویان ها از لحاظ موروفولوژی غیرطبیعی می باشند. حدود یک سوم از نمونه های سقط شده ی قبل از هفته 9 بارداری، فاقد رویان (anemberyonic) هستند. برخی موارد ساکهای خالی حاملگی و "Blighted Ova" در حقیقت نشان دهنده ی شکست حاملگی و متعاقباً جذب رویان است. نسبت بالایی از محصولات حاملگی سقط شده ی غیرطبیعی نتیجه یک فرایند انتخابی می باشند که باعث حذف حدود 95% ا زخطاهای سیتوژنی و مورفولوژی می شوند.
فراوانی اختلالات کروموزومی درمحصولات حاملگی سقط شده در سه ماهه اول تقریباً 60% است در حالی که در اواخر هفته ی 24 به 7% کاهش پیدا می کند. درصد اختلالات ژنتیکی در سقطهای فاقد رویان از این هم بالاتر است.
تری زومیهای اتوزومال، شایعترین اختلال کروموزمی هستند (51/9%)، اما فروانی نسبی هر نوع تریزومی بطور قابل ملاحظه ای متفاوت است. تریزومی 16، که درحدود یک سوم از سقطهای مربوط به تریزومی را شامل می شود، در نوزادان زنده متولد شده گزارش نشده و بنابراین قویاً کشنده است؛ فراوانی بعدی بترتیب مربوط به تریزومی 22 و 21 است. اختلالات کروزومی شایع دیگر به ترتیب نزولی شامل تریزومی X,45 (شایعترین اختلال کاریوتایپ منفرد)، تریپلوئیدی، تتراپلوئیدی، و موزائیسم می باشند.
عوامل مربوط به والدین (Parental factors)
در اکثر موارد، پدرو مادر دارای کورموزومهای طبیعی می باشند، لذا محصول حاملگی غیرطبیعی گهگاه و بطور اتفاقی بوجود می آید. در درصد کمی از موارد، یکی از والدین ناقل یک ترانسلوکاسیون متوازن (balanced translocation) است، و فرزندان این والدین ممکن است مکرراً سقط شوند. رسانه های تبلیغاتی تمایل به ایجاد این عقیده دارند که عوامل گوناگونی چون عفونت، پایانه های نمایش ویدئویی، کشیدن سیگار، مصرف قهوه، الکل، مواد شیمیایی، و داروها بطور قابل توجهی باعث افزایش miscarriage می شوند. در حقیقت، عوامل خارجی در تعداد معدودی از موارد باعث دفع محصولات حاملگی می شوند.
پاتولوژی
بیشتر سقط ها در کمتر از چند هفته بعد از مرگ رویان محصولات شبه رویان رشد نیافته اتفاق می افتند. در ابتدا خونریزی در دسیدوای پایه (decidua basalis)، با نکروز و التهاب درناحیه ی جایگزینی، رخ می دهد. محصول حاملگی بطور ناقص یا کامل جدا شده و به صورت یک جسم خارجی در داخل رحم در می آید.
انقباضات رحمی و دیلاتاسیون سرویکس معمولاً باعث خرج قسمت بیشتر محصول حاملگ یا همه آن می شوند. زمانیکه ساک باز میشود، غالباً در اطراف یک رویان له شده ی کوچک مایع یافت می شود، و یا ممکن است در ساک، رویان قابل رویت وجود نداشته باشد. از لحاظ بافت شناسی تخریب هیدورپیک پرزهای جفتی (Placental Villi) که بر اثر احتباس مایع بافتی بوجود می آید شایع است.
اشکال بالینی در درمان
درهر زنی در سنین باروری با خونریزی غیرطبیعی یا درد باید احتمال یک حاملگی تشخیص داده نشده را در نظر داشت. به هر زنی که به تازگی باردار شده است باید این آگاهی را داد که هر خونریزی واژنیال یا کرامپ رحمی را به پزشک خود اطلاع دهد. با توجه به اینکه درمان بستگی به عوامل متعددی دارد، روش آسان آن است که علایم بالینی سقط در زیرگروههای زیر در نظر گرفته شوند.
هر ترشح خونی واژینال یا خونریزی رحمی که در نیمه اول حاملگی اتفاق می افتد از قدیم تهدید به سقط محسوب می شده است. با توجه یه اینکه 25% از زنان باردار در ماههای اول بارداری درجات مختلفی از لکه بینی یا خونریزی را دارند، تهدید به سقط یک تشخیص شایع می باشد.
خونریزی مربوط به تهدید به سقط به طور تیپیک، کم بوده و از ترشحات قهوه ای تا خونریزی قرمز شوند متغیر است و ممکن است در سیر خود در چندین روز تکرار شود. تهدید به سقط معمولاً با کرامپ های رحمی یا سردردهای خفیف شروع می شود. در معاینه لگنی، سرویکس مسدود بوده و بافتی دفع نشده است. تشخیص های افتراقی شامل حاملگی خارج رحمی، حاملگی مول، پارگی های واژن، سرویسیت با خونریزی، زخمهای سرویکس، پولیپ و کارسینوما می باشند.
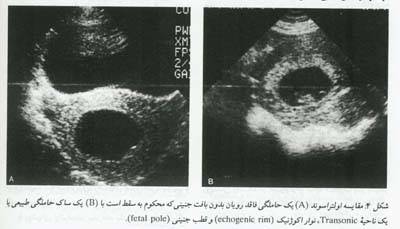
با روشهای اولتراسوند پیشرفته، یک محصول حاملگی زنده در هفته 5/5 بارداری قابل تشخیص است. توانایی دیدن رویان و حرکات قلب آن، ارزیابی و درمان تهدید به سقط را با دقت بیشتری امکان پذیر نموده است. دانستن سن دقیق حاملگی برای تفسیر مناسب ضروری است. یافته های اولتراسوند در هفته های 3 تا 4 حاملگی غیر قابل اطمینان اند و آنچه که رحم خالی بنظر می رسد و به اشتباه بصورت یک خونریزی داخل رحمی غیرطبیعی یا حاملگی خارج رحمی تفسیر می گردد، در حقیقت می توان مراحل اولیه یک حاملگی طبیعی باشد. اگر هر گونه شکی وجود دارد بهتر است با اندازه گیری ?-hCG و سونوگرافی مورد را پیگیری نمود. از 5 تا 6 هفتگی، کسیه زرده (yolk sac) و ساک حاملگی (gestational sac) را می توان توسط سونوگرافی واژینال مشاهده کرد، و فعالیت قلبی رویان را مدتی بعد از آن رویت نمود. اندازه غیرطبیعی ساک حاملگی و کیسه زرده، یک رویان کوچک نسبت به تاریخ حاملگی، و تعداد کم ضربان قلب رویان علائمی دال بر تمایل به دفع محصول حاملگی می باشند. بیش از 95% از حاملگی هایی که در آنها در هفته 8 حاملگی یک رویان زنده توسط سونوگرافی رویت می شود، تداوم پیدا می کنند. این رویان ها در هفته های بعدی احتمال مرگ و میر (mortality) پایینی دارند و اگر در هفته های 14 تا 16 حاملگی یک جنین زنده رویت شود، احتمال دفع محصولات حاملگی 1% خواهد بود.
اگر چه هیچگونه شواهد متقاعد کننده ای دال بر اثر گذاری روشهای درمانی بر سیر تهدید به سقط وجود ندارد، ولی هم دردی پزشک، همراه با ادامه حمایت ها و پیگیری های برای بیماران حائز اهمیت است. وقتی که محصول حاملگی زنده است این موارد شامل توضیح هوشیارانه درباره سیر بیماری و پیش آگهی جذب آن می شود. انجام یک رفتار خوش بینانه اما با احتیاط عاقلانه است زیرا تعداد کمی از این زنان بعداً با مرگ جنین یا رویان مواجه خواهند شد. به همین خاطر است که به بیماران توصیه می شود که در خانه یا نزدیک تلفن باقی بمانند تا بتواند حضور یا عدم حضور علائمی را گزارش دهند.
در صورت وجود خونریزی و کرامپ خفیف، بسته ماندن سرویکس، افزایش طبیعی مقادیر?HCG و مشاهده جنین یا رویان زنده در سونوگرام، باید نظارت بر بیمار (observation) را ادامه داد. اگر خونریزی و کرامپ به طور فزاینده ای افزایش پیدا کند نشانه ی پیش آگهی وخیم خواهد بود.
هم چنین با مقادیر منفی یا کاهنده ی HCG وجود شواهدی دال بر کاهش اندازه جنین یا رویان در سونوگرافی، تعداد ضربان قلب پایین، رحمی که درمعاینه لگن افزایش اندازه پیدا نکرده است، پیش آگهی خوبی وجود ندارد. اگر ارزیابی های دقیق بالینی نشان دهنده ی این باشند که محتویات بارداری زنده نمی ماند، راه های درمانی انتخابی شامل انتظار یا تخلیه رحم خواهد بود. در زنانی که در سونوگرافی دارای بافت داخل رحمی کمی می باشند، انتظار برای دفع خودبخودی محصولات حاملگی امکان پذیر است. در بیماران با مقادیر قابل توجه بافت داخل رحمی، کورتاژ رحمی الکتیو (elective) ممکن است باعث کاهش عوارض شود.
سقط ناکامل و اجتناب ناپذیر
(Inevitable and Incomplete Miscarriage)
دفع زودرس محصولات حاملگی، بخشی از یک فرایند است تا یک رخداد منفرد. سقط های ناکامل و اجتناب ناپذیر که در تقسیم بندیهای پیشین به دو موجودیت متفاوت تقسیم می شد، تصویر بالینی مشابه و درمانی یکسان دارند. زمانیکه خونریزی یا پارگی واضح پرده ها با درد و دیلاتاسیون سرویکس همراه باشد، سقط اجتناب ناپذیر خواهد بود. اما وقتی قسمتی از محصولات حاملگی از حفره رحمی عبور کرده و در حال خارج شدن از دهانه ی خارجی سرویکس (external os) یا همراه با خونریزی یا کرامپ واژن باشند، سقط ناکامل است. این واقعه وقتی در سه ماهه دوم رخ می دهد، احتمال باقیماندن بافت جفتی بیشتر خواهد بود. خونریزی ممکن است شدید بوده و گاهی باعث هیپوولمی شود. معمولاً معاینه دقیق واژن می تواند تشخیص را قطعی کند. بندرت اتفاق می افتد که یکی از محتویات بارداری سقط شده و قل باقیمانده طبیعی بارداری ار به پایان رسانده باشد. این حالت غیرمعمول می تواند در زمانی خونریزی در سه ماهه اول توسط سونوگرافی تشخیص داده شود. از جهت دیگر در سقط اجتناب ناپذیر و ناکامل، امکان بقای جنین وجود ندارد. برای جلوگیری از عوارض خونریزی یا عفونت مادر، تخلیه رحم توصیه می گردد.
در اکثر موارد، در بیماران سرپایی با استفاده از مسکن، بلوک پاراسرویکال، و تزریق وریدی نرمال سالین همراه با 10 تا 20 واحد اکسی توسین می توان به سرعت و با اطمینان کورتاژ ساکشن یا وکیوم را انجام داد.
اغلب سرویکس دیلاته است و محصول حاملگی را می توان به کمک فروسپس از کانال سرویکس و قسمت پایین رحم برداشت و هموستاز و همچنین انقباضات رحمی را تسهیل نمود. کورتاژ ساکشن با استفاده از فشار واکیوم و کورت پلاستیکی انجام می شود. در هنگام کورتاژ می توان بافت را در کورت و لوله ی ساکشن مشاهده نمود. در هنگام خارج نمودن، بافت کورت در جهت عقربه های ساعت 360 درجه چرخانده شده
و همین عمل در جهت مخالف عقربه های ساعت تکرار می گردد. زمانیکه احساس رنده کردن بوجود آمد و بافت بیشتری حاصل نشد نشاندهنده آن است که حفره اندومتر تخلیه شده است.
آماده بودن برای جلوگیری از مشکلاتی از قبیل حساسیتهای دارویی، آتونی رحمی (Uterine atony)، سوراخ شدن رحم (Uterine perforation)، تشنج، یا ایست قلبی، لازم است. مقدار هموگلوبین باید اندازه گیری شود ودر صورت بروز خونریزی باید تزریق خون انجام گیرد. اگر اقدامات انجام شده در اتاق اورژانس برای کنترل فوری خونریزی موفقیت آمیز نباشد، باید بیمار را برای معاینه زیر بیهوشی و تخلیه رحم، بهاتاق عمل منتقل نمود. پس از کورتاژ باید بیمار را برای چند ساعت تحت نظر قرار داد. بعد از تثبیت وضعیت، بیمار مرخص شده و به صورت سرپایی پیگیری می گردد. زنان Rh منفی، برای پیشگیری از ایمیونیزاسیون Rh باید 50?g یا 300?g استاندارد از ایمونوگلوبولین Rh دریافت دارند. بافت حاصله را برای تأیید وجود محصول حاملگی و رد کردن حاملگی خارج رحمی باید تحت معاینه قرار داد.
سقط کامل (Complete Miscarriage)
به تمام بیمارانی که از لحاظ تهدید به سقط تحت پیگیری قرار می گیرند، این آموزش داده می شود که تمامی بافتهای دفع شده را بمنظور بررسی نگهداری نمایند.
اندکی پس از خروج کامل محصول حاملگی درد و خونریزی متوقف خواهد شد. اگر تشخیص دقیق باشد نیاز به اقدامات بعدی نخواهد بود. در موارد مشکوک، سونوگرافی برای اطمینان از خالی بودن رحم کمک کننده است. در بعضی موارد برای اطمینان از تخلیه کامل رحم ممکن است نیاز به کورتاژ باشد. برداشت دسیدوای نکروز شده ی باقیمانده باعث کاهش شیوع خونریزی و کوتاهتر شدن زمان بهبودی می گردد.
سقط فراموش شده (Missed Miscarriage)
در این حالت، خروج محتویات بارداری، علیرغم گذشت زمان طولانی بعد از مرگ رویان، اتفاق نمی افتد. دلیل اینکه چرا تعدادی از رویان ها مرده به طور خودبخود سقط نمی شوند، مشخص نیست. در این حالت مشخصاً علایم بادرای متوقف می شوند، آزمایش حاملگی منفی شده، و ضربان قلب جنین با سونوگرافی قابل تشخیص نخواهد بود. درنهایت اکثر بیماران به طور خودبخود دچار سقط می شوند. بعلاوه درنیمه اول بارداری اختلالات انعقادی ناشی از باقی ماندن جنین مرده نادر است. اما باید متذکر شد که استرتژی صبر نوع تلاش عاطفی است که در این بیماران ترجیح می دهند که رحمشان تخلیه گردد. در حین سه ماهه اول بارداری، تخلیه حرم با کورتاژ ساکشن همراه با وارد کردن لامیناریا (اگر سرویکس بسته باشد) صورت می پذیرد. این عمل باید در بیمارستان همراه با تزریقات داخل وریدی مایعات و در دسترس بودن خون در مواردی که خونریزی واضح رخ می دهد، انجام شود.
در سه ماهه دوم باداری، تخلیه رحم می تواند با دیلاتاسیون و تخلیه (D&E) یا القاء زایمان با پروستاگلاندین E2 داخل واژنی یا میزوپروستول (Misoprostol) با نام تجاری cytotec انجام شود.
D&E نوع تکامل یافته روش سنتی دیلاتاسیون و کورتاژ (D&E) و کورتاژ واکیوم است. D&E بخصوص برای هفته های 13 تا 16 بارداری مناسب است، اگر چه برخی ماماها از این روش تا هفته 20 استفاده می کنند. معمولاً در ابتدا برای اجتناب از تروما، سرویکس با لامیناریا، دیلاته می شود و جنین و جفت با ساکشن و سایر ابزارها بصورت مکانیکی برداشته می شوند. در صورت استفاده از PGE2 واژینال، باید هر 4 ساعت یک شیاف 20 میلی گرم در قسمت بالا و پشتی دیواره واژن تا زمان خروج جنین و جفت کار گذاشته شود. برای کنترل اسهال و تهوع می توان بین 2/5mg تا 5mg از دیفنوکسیلات بصورت خوراکی و 10mg پروکلراپرازین (prochlorprazine) با نام تجاری compazine داخل عضلات تجویز کرد، و برای کنترل درد می توان از نارکوتیک ها یا بیهوشی اپیدورال استفاده کرد. در این وضعیت، باقی ماندن جفت نسبتاً شایع است و ممکن است نیاز به برداشت دستی و کورتاژ رحمی باشد. میزوپرستول (misoprostol) بصورت قرصهای 200mg که هر 12 ساعت در دهانه ی خارج سرویکس (external os) گذاشته می شود نیز مفید است.
سقط عفونی (Septic miscarriage)
سقط عفونی، یکی از مهمترین علل مرگ مادر است.
بعلت تغییر در قوانین سقط که باعث صدور مجوز برای پرشکان برای ختم حاملگی در حاملگیهای ناخواسته شده است، این عارضه از قبل کمتر دیده می شود. هر چند، هر سقط خودبخودی می تواند با عارضه ی عفونت همراه گردد. شایعترین شکل عفونت اندمتریت (endometritis) است اما می تواند به سمت پارمتریت (parametritis) و پریتونیت (peritonitis) نیز پیشرفت کند. علایم این بیماران تب، شکم حساس و درد رحم است. در مواردی شدید، عفونت موضعی به سمت سپتی سمی و شوک عفونی (septic shock) پیشرفت می کند. عفونت چند میکربی (polymicrobial) منعکس کننده فلور داخلی واژن بوده، شامل اشیرشیاکولی (Escherichia Coli) و دیگر باسیلهای گرم منفی، روده ای، هوازی، استرپتوکوک بتا همولیتیک گروه B، استرپتوکوک بی هوازی، گونه های باکتوئیدها، استافیلوکوک، و باکتری میکروآئروفیلیک می شوند.
ارزیابی اولیه و درمان سقط عفونی شامل چند مرحله است:
*معاینه فیزیکی و لگنی
*شمارش کامل سلول های خونی و الکترولیت ها، BUN، و کراتینین.
*گروه خونی و cross match
اسمیر از سرویکس و رنگ آمیزی گرم
*کشتهای هوازی و بیهوازی از اندوسرویکس، خون و نمونه های بدست آمده از محصولات حاملگی
*کارگذاری کاتتر فولی
*تزریق مایعات داخل وریدی (مانند سالین، رینگرلاکتات) از طریق یک آنژیوکت بزرگ
*تزریق زیر جلدی توکسوئید کزاز به مقدای 0/5ml در بیمارانی که قبلاً واکسینه شده اند، یا تزریق عمیق داخل عضلانی ایمونوگلوبولین کزاز
*رادیوگرافی ایستاده و خوابیده ی شکم برای تعیین هوای آزاد یا اجسام خارجی
درمان مناسب شامل تخلیه رحم و استفاده از آنتی بیوتیک های تزریقی قبل، در حین و بعد از برداشت بافتهای نکروزه توسط کورتاژ است. برداشت سریع بافت عفونی مهم است و باید در چند ساعت بعد از شروع آنتی بیوتیک های وریدی انجام شود.
رژیمهای آنتی بیوتیکی متعددی پیشنهاد شده اند، اما پوشش وسیع الطیف با دوز بالا، همانطور که در جدول 1 لیست شده است ضروری است. اگر چه بیماران مبتلا به سقط عفونی به درمان پاسخ مطلوب می دهند، ولی شوک عفونی یک عارضه جدی است که احتیاج به درمان قوی در یک مرکز مراقبتهای ویژه دارد.
درمان با یک دارو از هر گروه شروع می شود. رژیم توصیه شده براساس تأثیرات بالینی است و ممکن است در صورت در دسترس بودن یک آنتی بیوتیک جدید تغییر کند
جدول 1: رژیم های دارویی برای سقط عفونی
|
پوشش دادن ارگانیسم های هوازی و گرم مثبت های بی هوازی
|
|
1- پنی سلین G مائی: 5-4 میلیون واحد، داخل وریدی هر 6-4 ساعت (30-20 میلیون واحددر هر 24 ساعت)؛ یا
|
|
2- آمپی سلین، 2gr داخل وریدی هر 6-4 ساعت؛ یا
|
|
3- کلیندامایسین 600mg, (cleocin داخل وریدی هر 6 ساعت یا 900mg داخل وریدی هر 8 ساعت؛ یا
|
|
4- سفالوتین (keflin) (یا دیگر سفالوسپورینها)، 2gr داخل وریدی هر 6-4 ساعت (برای بیمارانی که به پنی سیلین حساسیت دارند، 10% احتمال حساسیت وجود دارد)؛ یا
|
|
5- ایمی پنم - سیلاستاتین (, (primax )(200-250mg هر 6 ساعت (در بیماران کمتر از 70kg یا بیماران با مشکل کلیوی باید دوز کاهش یابد ).
|
|
پوشش دادن ارگانیسم های هوای گرم منفی و مقاوم
|
|
1- جنتامایسین، 1-1/5 mg/kg داخل وریدی هر 8 ساعت (نفورتوکسیسیته و اتوتوکسیسیته را پایش کنید، در بیماران کلیوی دوز را کاهش دهید ).
|
|
2- ازترونام Azactam) 1-2gr) داخل وریدی هر 8-12 ساعت یا هر 6 ساعت در عفونت های شدید ( در بیمارانی که در اثر درمن با جنتامایسین دچار نفوتوکسیسیته شده اند، مقدار آنتی بیوتکی باید تغییر کند، در بیماران کلیوی دوز راکاهش دهید)؛ یا
|
|
3- ایمی پنم- سیلاسنتاتین (موارد قبلی را ببینید )
|
|
پوشش دادن ارگانیسم های بی هوازی گرم منفی
|
|
1- کلیندامایسین 600mg داخل وریدی هر 6 ساعت یا 900mg هر 8 ساعت؛ یا
|
|
2- مترانیدازول 1gr داخل وریدی دوز اولیه سپس 500mg هر 6 ساعت؛ یا
|
|
3- ایمی پنم- سیلاسنتاتین (موارد قبلی را ببینید )
|
سقط راجعه (Recurrent Miscarriage)
سقط راجعه که بصورت 3 یا بیشتر از 3 خودبخود و پشت سر هم در سه ماهه اول تعریف شده است، گریبانگیر حدود 1% زوجها می شود. اصطلاح سقط کننده های اولیه (Primary aborters) غالباً برای توصیف زنانی به کار می رود که هرگز حاملگی موفقی نداشته اند و سقط کننده های ثانویه (secondary aborters) به زنانی گفته می شود که سقط های مکرر آنها متعاقب یک تولد زنده صورت گرفته است. برای زنامی که دارای سقط ها متعدد همراه با حاملگی های طبیعی بینابینی هستند، طبقه بندی خاصی وجود ندارد. این مورد قبول همه است که برای یافتن علل احتمالی دفع مکرر محصولات حاملگی (recurrent pregnancy Loss-RRL) در اکثر بیماران بعد از سه بار سقط پشت سر هم و در زنان با سن بالای 30 تا 35 سال با دو بار سقط اندیکاسیون بررسیهای تشخصی وجود دارد. در مورد درمان زوجهای مبتلا به RPL، اختلاف نظر وجود دارد. در دهه گذشته در مقالات علمی ـ گزارشی، توجه زیادی به این قضیه شده است. علیرغم تبلیغات گسترده در این زمینه شواهد ناچیزی وجود دارد که تغذیه ضعیف، عفونت ها، دیابتهای تشخیص داده نشده، مواد توکسیک، یا آسیب های روانی، از عوامل اتیولوژیک مهم باشند.و به این ترتیب در طول سالها آزمایشهای قبلی گشتند. آخرین و جدیترین فرضیات شامل آنتی بایدهای ضد تیروئیدی، غلظت بالای هورمون لوتئینیزه کننده در مرحله فولیکولی، عامل آمبریوتوکسیک مادری موجد در گردش خون، و نسبتهای غیرطبیعی زیر مجموعه های لنفوسیتی (سطوح بالای CDS6) است.
آنالیز بسیار دقیق تمایم آزمونها خارج از حیطه این فصل می باشد، اما جنبه تئوری مکانیسم دفع محصولات حاملگی و رابطه هر کدام از اینها کماکان باقی است. تا زمانیکه براساس مطالعات دقیق درمانهای مؤثر مشخص نشده است، انجام آزمایشات غربالگری، کاربرد کمی در ارزیابی روتین بیماران مبتلا به RPL دارد. بطور کلاسیک، مطالعات عوامل آناتومیک، هورمونی، ژنتیک و اتوایمیون توصیه شده است.
اختلالات ساختاری رحم (Structural uterine defects)
هیسیتروسالپنگوگرافی، MRI، هیستروسکوپی، و لاپاروسکوپی در تشخیص دیواره دارد (Septate Uterus، دیگر آنومالهیای مولرین anomalies mullerian)، اختلالات رحمی مربوط به تماس دی اتیل استیل بسترول، میومهای زیرمخاطی و چسبندگیهای داخل رحمی کمک کننده هستند. پیش آگهی در بیماران مبتلا به آنومالی ها مولرین برای حاملگی های موفقیت آمیز، بستگی به نوع مالفورماسیون دارد، اختلالات فیوژنی نامتقارن، بدترین پیش آگهی رادارند و رحم جداره دار، دوشاخه و دی دلفیک (didelphic) به ترتیب دارای پیش آگهی بهتری هستند. در بیماران مبتلا به RPL، شیوع این اختلالات آناتومیک تقریباً 15-10% است. علت دفع محصولات حاملگی در زنان مبتلا به آنومالیها رحمی نامشخص است، البته کاهش خونرسانی و تداخل با جایگزینی طبیعی و placentation و کاهش اندازه حفره رحم از دلایل ذکر شده می باشند.
در اکثر موارد، برداشت دیواره رحم توسط هیستروسکوپ، جایگیزن متروپلاستی (metroplasty) شکمی شده است. این عمل می تواند در شرایط سرپایی انجام شود و نیاز به انجام سزارین را کمتر می کند. درصد تولد زنده بعدی بیش از 80% است. رفع چسبندگی و برداشت میومهای زیرمخاطی نیز می تواند از طریق هیسترسکوپی انجام شود.
مسائل غدد داخلی (Endocrine problems)
نقصان فازلوئتال (luteal-phase deficiency) اصطلاحی است که بر سر آن اختلاف نظر وجود دارد و به عملکر غیرطبیعی تخمدان با تولید ناکافی پروژسترون یا اثر نامناسب پروژستورن روی اندومتر اشاره دارد. بیماران مبتلا به LPD مشخصاً دارای سیکل های کوتاه قاعدگی، فواصل کمتر ار 14 روز بعد از تخک گذاری، و نازایی ثانویه با دفع
مکرر زودرس محصولات حاملگی هستند. علت دقیق دفع محصولات حاملگی در بیماران مبتلا به LPD مشخص نیست، اما ترشح پروژسترون توسط جسم زرد برای حمایت اندومتریوم، تا زمان تولید پروژسترون توسط جفت در حدود هفته های 6 تا 8 حاملگی، لارم است. علل زمینه ساز LPD شامل کاهش هورمون رها کننده گنادوتروپین (Gnrh)، کاهش هورمون تحریک کننده فولیکول (FSH)، هورمون لوتئینیزه کننده ناکافی (Inadequate LH) استرئیدوژنژ (steroidogenesis) ناکافی تخمدان، و اختلالات گیرنده اندومتری است.
بعلت عدم توافق بر مشخصه های لازم برای تشخیص، شیوع واقعی این حالت نامشخص است. آزمایشاتی که موردقبول می باشند. عبارتند از: بیوپسی اندومتر و اندازه گیری پروژسترون سرم در فازلوتئال. هر دو آزمایش برای اواخر فاز لوتئال زمانبدی شده اند. بیوپسی اندومتر از لحاظ بافت شناسی تاریخ گذاری شده است و یک فاصله بیش از 2 تا 3 روز مشکوک در نظر گرفته می شود.
به علت طبیعی بودن اسپورادیک این تأخیر اندومتر از لحاظ بافت شناسی، در زنانی که هیچگونه مشکل باروری ندارند، باید با بیوپسی مکرر نتیجه را قطعی نمود.
سابقه جایگزین کردن پروژسترون برای LPD به مشاهداتی برمی گردد که در آن با برداشت جسم زرد به روش جراحی قبل از هفته 6 تا 8 باردای، سقط خودبخود رخ داده است. شایع ترین درمان پیشنهاد شده مصرف 25mg پروژسترون به صورت شیاف داخل واژن صبح و شب بعد از تخمک گذاری و ادامه آن تا زمان شروع قاعدگی یا در 8 تا 10 هفته حاملگی است. دوزها مشابه خوراکی پروژستورن میکرونیزه شده (microminized progestrone) نیز مورد استفاده قرار گرفته اند. درصد حاملگیهای موفقیت آمیز بیش از 90% گزارش شده است، اما مطالعات کنترل موجود نیست و ممکن است یک سقط فراموش شده اتفاق افتاده باشد. کلومیفن و دیگر عوامل تخمک گذاری نیز برای بهبود تکامل فولیکولی و عملکرد جسم زرد مورد استفاده قرار گرفته اند، اما نتایج متغیر بوده است.
اختلالات کروموزومی
آنومالیهای کروموزمی والدین در تقریباً 5% زوجهای مبتلا به RPL یافت شده است. آزمایشات سیتوژنیک از پدر و مادر برای پیش بینی تکرار سقط، کمک کننده بوده و در عین حال اساس مشاوره ژنتیک را تشکیل می دهد. بیشترین اختلالات ترانسلوکاسیون های متوازن هستند،که دو سوم آنها جابجایی دو طرفه (reciprocal) و یک سوم آنها الگوی رابرتسونین (Robertsonian) را نشان می دهند. درصد سقط خودبخود در زوجهای مبتلا به ترانس لوکاسیون متوازن از 50% در جابجایی دوطرفه تا 25% در رابرتسونین متغیر است. تمام زوجهای مبتلا به اختلالات کروموزومی باید برای رد یک اختلال جدی کروموزومی جنین در هر حاملگی بعدی تحت آمنیروسنتز ژنتیکی یا نمونه گیری از chorionic villus قرار گیرند. اختلالات کروموزومی معمولاً دلیلی بر رد تمایل به حاملگی های بعدی نیستند، زیرا بیشتر زوجها نهایتاً فرزندان طبیعی خواهند داشت. برای موارد نادر جابجایی رابرتسونین همولوگ که از حاملگی موفقیت آمیز جلوگیری می کند، امکانات درمانی شامل artificial donor insemination، لقاح خارجی، اووسیت دهنده و adoption وجود دارد.
آنالیز کروموزومی محصولات حاملگی نیز از لحاظ بالینی بخصوص در ارزیابی علت شکست یک رژیم درمانی کمک کننده است. جهش های مولکولی که ممکن است در آینده به عنوان علت سقط مکرر شناخته شوند، شامل جهش های کشنده تک نقطه ای (lethal, single-point)؛ احتمالاً متصل به ژنهای MHC؛ جهش در ژنهای کدکننده محصولات مهم برای تکامل طبیعی؛ جهش های ژنهای homebox که کنترل کننده تنظیم رونویسی (Transcription) هستند؛ جهش هایی که منجر به اختلالت شدید متابولیک و مرگ رویان می شوند؛ و اختلالات پروتوانکوژنها (protooncogenes) و انکوژنها (oncogenes) می شوند.

اختلالات اتوایمیون
سندرم آنتی فسفولیپید (Antiphospholipid syndrome-APS) از پیش از یک دهه قبل بعنوان یک عامل ثابت شده در دفع محصولات حاملگی شناخته شده استتقریباً 5% زنان مبتلا به RPL دارای ضدانتقاد لوپوس (Lupus Anticoagulant-LA)، مقادیر متوسط تا زیاد آنتی کاردیولیپین (anticardiolipin-aCL)، یا هر دو می باشند. این آنتی بایدهای آنتی فسفولیپیدی اکتسابی توسط یک محرک ناشناخته در یک وضعیت تنظمی ایمنی انحرافی بوجود آمده اند. مقادیر پایین IgM یا IgG آنتی کاردیولیپین از شواهد مشکوک هستند. نشانه های اندکی مبنی بر شرکت دیگر آنتی بایدهای آنتی فسفولیپیدی در درمان بیماران RPL وجود دارد.
مهمترین یافته در اینگونه بیماران، درصد بالای مرگ در اواخر سه ماهه اول یا دوم در جنین است که فعالیت قلبی وی تشخیص داده شده است. بیماران با مقادیر بالای aCL یا یک تاریخچه قبلی از مرگ جنینی، در بالاترین حد خطر برای دفع جننینی دیگر هستند. به نظر می رسد علت مرگ جنینی، واسکولوپاتی (vasculopathy) دسیدوا باشد که منجر به انفارکتوس و خونرسانی ناکافی به جفت می شود. ترومبوزهای داخل ویلوسی نیز از دیگر علل ذکر شده اند. ولی این ضایعات غیراختصاصی هستند، و پاتولوژی همیشه برای توضیح علت مرگ جنین کافی نیست. مکانیزمی که توسط آن aCL ممکن است باعث واسکولوپاتی و اسیدوز و مرگ جنین شود ناشناخته است. عدم توازن بین تولید ترومبوکشان و پروستاسایکلین موضعی که باعث انقباض عروق می شود، تجمع پلاکتی، ترومبوزهای داخل عروقی، کاهش فعالیت پروتئین C، و کاهش تروفوبلاست انکسین Trophoblast annexin V) V) از علل مفروض می باشند.
وجود LA یا aCL مثبت یک شاخص تغییر ناپذیر پیش آگهی بد نیست، و تعدادی از بیماران بدون هیچگونه درمان پزشکی خاصی حاملگی های موفق داشته اند. ولی برخی از گزارشات پیشنهاد می کنند که زنان مبتلا به APS و دفع محصولات حاملگی قبلی می توانند در خیلی از حاملگی های بعدی برای افزایش شانس زایمان یک نوزاد زنده، تحت درمان قرار گیرند.
در حال حاضر مشخص شده است که هپارین با مقادیر کم آسپرین، مؤثرترین و مطمئن ترین روش درمان است(جدول 2) . یک رژیم درمانی شامل مصرف روزانه مقادیر کم و تک دوز آسپرین در طول حامگی می شود. تزریق زیرجلدی هپارین (7500 واحد هر 12 ساعت) و سه ماهه اول یک حاملگی که زنده بودن نوزاد در آن تأیید شده باشد شروع می شود، و تا زمان تنظیم دوز داروهای ضدانعقادی در سه ماهه دوم افزایش پیدا می کند. از مصرف همزمان کورتیکواستروئیدها و هپارین باید اجتناب شود، زیرا مشخص نشده است که اثر ناشی از همراهی این دو روی تولد یک نوزاد زنده بهتر از مصرف آنها به تنهایی باشد.
امکان مقایسه بین مطالعات مختلف به علت تفاوت در عوامل انتخابی، موارد تشخیصی و رژیمهای درمانی وجود ندارد.
درعین حال تعددی از موارد استئوپروز شدید همراه با شکستگی رخ داده است. استفاده از مقادیر بالای ایمونوگلوبولین های داخل وریدی بعلت گزارشات دال بر حاملگیهای موفقیت آمیز با مقادیر کاهش یافته aCL، توجه بسیاری را برانگیخته، اما مطالعات کنترل انجام نشده است. بیماران مبتلابه APS، حتی در صورت درمان، احتیاج به مراقبتهای قبل از زایمان دارند).
اختلالات ترومبوفیلیک (Thrombophilic disorders)
اخیراً RPL با حالتهای پیش انعقادی (hyper hyperhomocysteinemia ,cohulable) و کمبود در فاکتور xll فعال (فاکتور Hageman) ربط داده شده است. کمبود آنتی ترومبین III، پروتئین C یا پروتئین S هم با درصد بالای سقط سه ماه اول و هم مرگ جنینی همراه می باشند، در صورتی که جهش فاکتور V لیدن (Leiden) باعث افزایش خطر دفع محصولات حاملگی در سه ماهه دوم می شود. فاکتور V غیرطبیعی مقاوم به اثرات ضدانعقادی پروتئین C فعال شده از لحاظ تعداد، مهمترین علت بیماری ترومبوآمبولیک فامیلی است. این حالت غالباً با جهش فاکتور V لیدن در ژن فاکتور V همراه است و تقریباً در 2 تا 5 درصد از جمعیت طبیعی دیده می شود. هنوز مشخص نیست که کدامیک از بیماران RPL بمنظور غربالگری برای thrombophilias مناسب هستند و طرح مناسبی برای مشخص کردن اینکه آسپرین یا ضدانعقاد درمانی (anticoagulant therapy) توانایی کاهش خطر حاملگی در زنان را دارند یا نه، ضروری است.
علل ایدیوپاتیک
بعلت اینکه در اکثر موارد مبتلا به RPL علیت مشاهده نشده است، عوامل آلوایمیون را برای آن فرض کرده اند. این موارد هنوز ثابت نشده اند، خصوصاً اینکه دانش کمی در مورد مکانیزم پیشگیری از واکنش پس زدن ایمنی در محتویات بارداری در یک حاملگی نرمال وجود دارد )
گزارشات اولیه حاکی از آنند که تطابق HLA بین زوجها، عدم وجود آنتی بادیهای لکوسیتوتوکسیک (leukocytotoxic) مادری، یا عدم وجود آنتی بادیهای بلوک کننده مادری، با RPL رابطه داشته اند. اهمیت این عوامل هنوز اثبات نشده است، و انجام این آزمایشات پرهزینه از لحاظ بالینی اندیکاسیون ندارد. تحقیقات کنونی روی عوامل سرکوب کننده ایمنی تروفوبلاست یا دسیدوای موضعی مانند سیتوکینها، عوامل رشد، هورمون ها، آنزیمها، و پروتئینهای اندومتر متمرکز شده است. بنظر می رسد که برخی از این عوامل فعال ایمنی برای جایگزینی و رشد و نمو اولیه رویان و جفت ضروری باشند و برخی دیگر ممکن است در صورت بروز باعث سقط شوند. آزمایشان بالینی عملی قابل دسترس برای این عوامل وجود ندارد، و تشخیص RPL وابسته به عوامل آلوایمیونی یکی از موار استثناء است.اگر چه هیچ مکانیسم آلوایمیونی بطور قطع بعنوان علت RPL در انسان مشاهده نشده، چندین نوع ایمنی درمانی (immunotherapy) پیشنهاد شده است. اساساً تمایل به بهبود تحمل ایمنی مادر (maternal immunotolerance) در سقط کننده های مکرر، براساس مشاهداتی است که در آن ها مشخص شده است. تزریق خون قبل از پیوند باعث کاهش پس زدن عضو آلوگرافت شده است و هم چنین در مدلهای حیوانی که قبلاً با سلوهای طحال ایمن شده بودند، عمومی ترین دستور، تزریق لکوسیتهای شوهر است اما در مورد مقدار، روش یا اندیکاسیون های درمان توافق نظر وجود ندارد. ایمن سازی با استفاده از لکوسیتهای زنده همان خطرات تزریق خون مانند، هپاتیت، ایدز و عفونتهای ویروسی سیتومگال را بدنبال دارد. واکنش ها (Reactions) شایع نیستند اما شامل زخم و قرمزی در محل تزریق، واکنش پوستی شبه میزبان در برابر پیوند (grft-versus-host)، تب، آلوایمیونیزاسیون لکوسیت و پلاکت مادری، حساس سازی گروه خونی (Blood type Sensitization) می باشند.
با توجه به اینکه بدون درمان هم شانس حاملگی موفقیت آمیز وجود دارد، مؤثر بودن این درمان غالباً مورد سؤال است. وقتی که اطلاعات بدست آمده از آزمایشات تصادفی آینده نگر (prospective randomized) با یک متاآنالیز اخیر ترکیب می شوند، به نظر می رسد که ایمن سازی با لکوسیت اثر کمی داشته باشد. میزان تولد زنده برای ایمن شده ها 68 و برای گروه کنترل 61 درصد بوده است. متاآنالیزهای دیگری نیز تکمیل گشته اند و نتایج قویاً وابسته به ورشهای مورد استفاده برای آنالیز بودند). هنوز مشخص نیست که آیا آلوایمیونزیاسیون با لکوسیت پدری یک روش درمانی مناسب برای بیماران مبتلا به RPL بدون علت مشخص است یا خیر، و پاسخ قطعی ممکن است بدنبال یک کارآزمایی تصادفی چندمرکزی (completed multicenter randomized tiral) حاصل شود. تزریق داخل وریدی ایمونوگلوبولین بعنوان یک جایگزین درماین دیگر در بیماران مبتلا به RPL بدون علت مشخص پیشنهاد شده است.
گزارش نتایج سه آزمون کنترل شده گیج کننده بوده اند. با این حال بنظر می رسد که این درمان بیشتر از ایمن سازی با سلول پدر مؤثر نباشد.
تا زمانیکه مؤثر بودن و اطمینان دراز مدت کاملاً مشخص شود، باید تفسیر نتایج با احتیاط صورت گیرد.
در جدول 3 یک طرح برای درمان مؤثر و با صرفه از نظر اقتصادی خلاصه شده است. درمان عوامل غیرایمنی مادر نیز مؤثر است و در بیمارانی که خوب انتخاب شده باشند نتیجه خوبی عاید می شود. اگر اقدامات اولیه منفی باشند، براساس سن بیمار، وضعیت و خواستهای زوج، اقدام به بارداری بدن انجام هر گونه روش درمانی پیشنهاد می گردد. البته اگر بیمار دارای سالهای باروری باقیمانده کم، مشکل نازایی، یا چندین سقط باشد، اقدامات زودتر و جدی تری نیاز است. اگر ارزیابی ایمن و ایمنی درمانی آزمایشی مدنظر قرار گرفته باشد، شاید بهتر باشد که بیمار به مراکز تحقیقاتی قانونی ویژه ارجاع شود.
همدردی پزشک با بیمار بسیار مهم است. بوجود آوردن حس اعتماد و ارتباط و درک صادقانه از فشار و درد تجربه شده توسط این زوجها باعث می شود که بحث های دقیق و با حضور ذهنی کافی با بیمار و شوهرش انجام شود.
تاریخچه
|
|
|
شکل دفع محصولات حاملگی و زمان آن و اینکه آیا جنین زنده موجود بوده است؛ سرنخ های مشکوک از بیماری خودایمنی؛ تماس غیرمعمول با توکسین های محیطی، داروها، عفونت ها؛ بیماریهای قبلی زنان یا جراحی قلبی، شامل دیلاتاسیون و کورتاژ؛ درمانها و آزمونهای تشخیصی قبلی را تعیین کنید . (a)
|
|
$معاینه بالینی
|
|
اختلالات درمعاینه لگنی، شامل یافته های مشکوک به سرویسک غیرطبیعی، تماس با دی اتیل استیل بسترول، یا آنومالیهای رحمی
|
|
$آزمایشات
|
|
هیستروسالپنگوگرام
|
|
بیوپسی اندومتر در فاز لوتئال
|
|
آنالیز کوروموزم والدین
|
|
آزمایش غربالگری برای ضدانعقاد لوپوس و ضدکاردیولیپین (lupus anticoagulant & anticardiolipin)
|
|
دیگر آزمایشات مورد نیاز براساس تاریخچه و معاینه بالینی
|
|
a= بررسی سونوگرافی در هفته 6 حاملگی بعدی و آنالیز کروموزومی محصولات حاملگی در هر سقط خودبخودی
|
نارسایی سرویکس (cervical incompetence)
نارسایی سرویکس، که مناسبتر است دیلاتاسیون زودرس سرویکس نامیده شود، یکی از علل مهم دفع محصولات حاملگی در سه ماهه دوم است. مشخصیه این حالت در بحث زایمان حاصل از دیلاتاسیون بدون درد و تدریجی سرویکس همراه با برآمدگی (bulging) یا پارگی پرده ها وبیرون افتادن جنین دیده می شود. معمولاً جنین آنقدر نارس است که زنده نمی ماند. دفع محصولات حامگلی ناشی از اختلال سرویکس معمولاً در سه ماهه دوم اتفاق می افتد و تصور می شود که می توان به طور کامل و مشخص آن را از سقط سه ماه اول با دردهای زایمانی زودرس در سه ماه دوم جدا کرد. این حالت از عوامل مختلفی ناشی شده، علائم بالینی مشخصی داشته و نیاز به درمانهای متفاوتی دارد. سقط و دردهای زایمانی زودرس شابع بوده، اما دیلاتاسیون زودرس سرویکس در سه ماهه میانی حاملگی (mid trimester نسبتاً نادر است.
سرویکس برخلاف بقیه رحم که از ساختمانی ماهیچه ای ساخته شده است، داری بافت پیوندی است.
شکل 7:odds,ratioمصرف دارو نما در مقایسه با عدم درمان در برابر ایمن ساز ی به لکو سیت پدری بر اساس اطلاعات حاصل از آزمونهای تصادفی گذشته نگر .اگر چه نسبت تولدزنده در ایمن سازی با لکو سیت های پدری از لحاظریاضی فقط در سه آنالیز از پنج آنالیز معنی دار است .
علت نارسایی سرویکس مبهم است و عوامل اتیولوژیک مختلفی برای آن در نظر گرفته اند. بنظر می رسد مواردی چون جراحی یا تروما به سرویکس مانند D&C، آمپوتاسیون ، کونیزاسیون، کوتریزاسیون، برداشت با جراحی قوس الکتریکی (Loop Electrosurgical Excision Procedure-LEEP) یا زایمان تروماتیک، در برخی از بیماران از علل نارسایی سرویکس باشند. در دیگر موارد بنظر می رسد که نقایص ساختمانی مادرزادی سرویکس، آنومالیهای رحم، یا رشد غیرطبیعی سرویکس که با تماس دی اتیل استیل بسترول در رحم همراه است، نقش دارند.
در مورد تشخیص نارسایی سرویکس توافق اندکی وجود دارد بجز در مورد اینکه نارسایی سرویکس از مواردی است که نیاز به ارزیابی دقیق برای رد دیگر علل دفع محصولات حاملگی درنیمه حاملگی دارد. علل دیگر شامل، جفت سرراهی، کوریوآمینونیت و آنومالیهای رحم می شوند، اما معمولاً علایم بالینی متفاوتی دارند. اینکه آیا می توان این حالت را تشخیص داد، چه در زنان غیرحامله با روشهای اندازه گیری قطر کانال اندوسرویکس یا در مراحل اولیه بارداری با یافته های سونوگرافی، جای سؤال دارد. تشخیص قطعی نارسایی سرویکس فقط با دیدن بیرون زدگی پرده ها از میان سرویکس تقریباً دیلاته شده در بیماری که در نیمه های حاملگی قرار داشته دچار دردهای زایمانی نشده است، امکان پذیر است. یک تشخیص فرضی زمانی قابلیت اطمینان بیشتری دارد که سابقه دیلاتاسیون آرام تکرار شده سرویکس و متعاقباً پارگی پرده ها و زایمان تقریباً بدن درد و سریع یک نوازد نارس وجود داشته باشد. در معاینه سرویکس یک زن غیرباردار، ممکن است سرویکس کوتاه، یا تغییر شکل یافته همراه با بریدگیهایی باشد که بعضی اوقات تا فورنیکس واژن ادامه پیدا می کند.
اگر چه استراحت، وسایل داخل واژنی گوناگون و عوامل دارویی با موفقیت های زیادی استفاده شده اند، درمان مورد قبول برای سرویکس نارسا جراحی است. روشهای گوناگونی شرح داده شده اند، اما شایعترین روش های مورد استفاده مک دونالد و شیرودکار هستند. این روشها بصورت داخل واژنی ومعمولاً تحت بیحسی موضعی انجام می شوند و باعث تقویت سرویکسی در سطح دهانه داخلی (internal os) می گردند. اگر بافت سرویکس برای قراردادن سر کلاژ واژنی ناکافی باشد باید عمل جراحی از طریق شکم صورت گیرد.
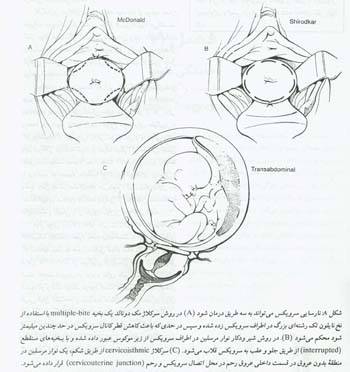
کارگذاری بخیه های پشتیبان معمولاً در اواخر سه ماه اول و بعد را تشخیص جنین زنده توسط سونوگرافی، بعد از برطرف شدن خطر سقط و قبل از شروع دیلاتاسیون سرویکس، صورت می گیرد.
اغلب تایخچه بیمار کلاسیک نیست و تعیین دخداد دیلاتاسیون زودرس سرویکس درحاملگی بعید، مشکل است. معمولاً این بیماران به منظور تشخیص پتانسیل تغییر سرویکس، تحت معاینات مکرر واژینال و سونوگرام های پشت سر هم قرار می گیرند. سونوگرافی می تواند در تعیین اندازه سرویکس مورد استفاده قرار گیرد، اما مشخص نیست که در صورت غیرطبیعی بودن یا نبودن نتایج سونوگرافی، آیا تفاوتی در نتایج حاملگی وجود خواهد داشت یاخیر. مطالعات ابتدایی پیشنهاد می کنند که تکنیک های تشخیصی ممکن است یک مسأله جنبی مفید در پیگیری بیماران با خطر نارسایی سرویکس باشند.
کارگذاری سرکلاژ در سه ماه دوم بعد از بوجود آمدن تغییرات سرویکس در بعضی مواق ضرورت پیدا می کند اما کمتر مؤثر است. اگر شکی در تشخیص وجود داشته باشد، مامبرآنها پاره شده باشند، و خونریزی واژینال و دردهای کرامپی قسمتی از علایم بالینی باشند، نباید از این عمل جراحی استفاده شود.
شواهدی موجود نیست که آنتی بیوتیکهای بعد از عمل جراحی، پروژسترون، یا مواد توکولیتیک (tocolytic agents) بعنوان درمان کمکی مفید باشند. اگر در هر زمانی پرده ها پاره شوند یا درد زایمان شروع شود، برای جلوگیری از کوریوآمنیونیت، سپسیس، پارگی سرویکس و یا پارگی رحم باید سرکلاژ برداشته شود. از طرف دیگر اگر تکامل جنین کامل شده باشد، معمولاً بعد از هفته 37 بارداری، باید بخیه ها را برداشت که معمولاً متعاقب آن شروع دردهای زایمانی و وضع حمل به سرعت انجام می شود. اگر بیمار مایل به حاملگیهای بعدی باشد، برخی از پزشکان سرکلاژ را نگهداشته و زایمان را از طریق سزارین انجام می دهند.
مؤثر بودن سرکلاژ غالباً حتی در زنانی که علایم بالینی کلاسیک داشته اند، مورد بحث بوده است. با این حال، وقتی که انتخاب بیمار به صورت دقیق انجام شده باشد، این نوع از درمان تا 90- 80% در جلوگیری از زایمان جنین نارس موفق است. تفاوت ناچیزی در درصد بقای جنین بین تکنیکهای شیرودکار و مک دونالد موجود است. در بیمارانی که زایمان نارس قبلی داشته اند و شواهد متقاعد کننده کمتری برای نارسایی سرویکس وجود دارد، نیز می توان بعنوان پیشگیری از روشهای فوق استفاده کرد. هر چند در این گونه موارد، مطالعات تصادفی گذشته نگر تفاوتی را در نتیجه حاملگی بین گروهای درمان شده و درمان نشده نشان نداده اند.
خلاصه نکات
|
*سقط شایعترین عارضه حاملگی بوده، شایعترین علت آن اختلالات کروموزومی محصول حاملگی است .
|
|
*اولتراسوند در تعیین زنده یا مرده بودن رویان کمک کننده است. درمان مناسب پیشرفته شامل تحت نظر گرفتن بیمار یا تخلیه رحم است .
|
|
*دفع مکرر محصولات حاملگی غالباً بر پایه اختلالات مادری است که می تواند با آزمایشات استاندارد تشخیص داده شود. ولی در مورد جلوگیری از سقطهای بعد با آزمونهای ایمونولوژی و ایمنی درمانی پیشنهاد شده، اختلاف نظر وجود دارد
|
منبع:نشریه مامایی و بیماریهای زنان،نفورث،جلد اول
/ک