جراحی به روش آندوسکوپی
Endoscopic Surgery
آندوسکوپی در ژنیکولوژی شامل استفاده از تلسکوپ کوچکی برای مشاهده حفره صفاقی (لاپاروسکوپی) و حفره داخل رحمی (هیستروسکوپی)است.این تکنیک ها از روشهایی که در ابتدا جهت مقاصد تشخیصی استفاده می شدند به سیستم های پیچیده ای برای انجام جراحی های بزرگ متحول شده اند.هدف جراحی آندوسکوپی فراهم آوردن نتایج عالی برای بیماران همراه با کاهش مدت بستری در بیمارستان تسریع در زمان بهبودی و هزینه کمتر است.این مفهوم منجر به ایجاد اصطلاح توصیفی تحت عنوان «جراحی با حداقل تهاجم» شده است. گر چه مزایای بعضی اعمال آندوسکوپی بوضوح نشان داده شده، در سایر زمینه ها از نظر صرفه اقتصادی و پیامدهای دراز مدت هنوز اطلاعات کافی وجود ندارد.
لاپاروسکوپی
برای انجام لاپاروسکوپی مطمئن و موثر، جراح باید به اندازه کافی در تکنیک های جراحی لاپاروسکوپی از جمله دانش و تجربه در مورد استفاده از ابزارهای لاپاروسکوپی برای دستکاری بافت ها و اطلاعاتی در مورد منابع انرژی که برای جدا کردن نسوج و دستیابی به هموستاز بکار می روند مهارت داشته باشد.
ابزارگذاری برای لاپاروسکوپی جراحی
از آنجا که برای عمل لاپاروسکوپی ابزارهای تخصصی بسیاری مورد نیاز است، برای جلوگیری از سردرگمی استفاده از یک سینی ابتدایی لاپاروسکوپی و غیر لاپاروسکوپیک که معمولاً مورد استفاده قرار می گیرند،مفید است.اجزای ابتدایی و پایه لاپاراسکوپی عبارتند از یک لاپاروسکوپ، واحد دمنده،ویدئو،منبع نور،تروکارها، قیچی ها، فورسپس ها، سوزن گیرها، شستشو دهنده و مکنده،گیره ها (staplers)، گیره های (clips) عروقی و جابجا کننده رحم.ابزارهای غیر لاپاروسکوپیک شامل آنهایی هستند که برای ایجاد برش با تروکار (Scalpel)، کمک به خارجی کردن نمونه های نسجی (کلامپ کوخر) و بستن برش های حاصل از تروکار (سوزن گیر،قیچی ها،رتراکتور s) بکار می روند،ابزارهایی که کمتر مورد استفاده قرار می گیرند را باید در محلی معین که در دسترس باشند نگهداشت. مدیریت این کار باید با یک تیم تخصصی اطاق عمل باشد.
لاپاروسکوپی
لاپاروسکوپ یک تلسکوپ خشک و غیر قابل انعطاف به قطر 11-2 میلی متر است که حاوی فیبر نوری بوده که نور را از منبع نور به حفره صفاقی منتقل می کند (شکال1).ممکن است لاپاروسکوپ دارای یک مجرا یا کانال باشد که از طریق آن ابزارهایی را چون فیبرلیزری برای برش یا خشک کردن و یا فورسپس های دو قطبی برای کوتر کردن لوله ها،عبورداد.
واحد دمنده (Insufflator)
واحد دمنده (Insafflator) تحویل گاز کربنیک (Co2) را برای ایجاد فیزوپریتوئن به منظور ایجاد دید بر عهده دارد. هنگامی که دی اکسید کربن بداخل حفره صفاق جریان دارد،می توان شاخص ها را برای کنترل جریان و فشار تنظیم نم ود.

شکل 1: سه نمونه آندوسکوپ با اندازه های متفاوت که در لاپارسکوپی بکار می روند:2میلی متری (بالا)،5 میلی متری (وسط)،و 10 میلی متری (پایین ).لاپاروسکوپ 10 میلی متری واجد یک مجرای عملی است و چشمی جداگانه دارد.
واحد ویدئو
اگرچه برای انجام لاپاروسکوپی ضرورت وجود واحد ویدئو بطور مطلق نیست،این واحد به جراح اجازه می دهد که بجای اینکه برای دیدن از طریق لاپاروسکوپ به جلو خم شود،بصورت مستقیم بایستد.بعلاوه به دستیار جراح و سایر کارکنان اطاق عمل اجازه می دهد که محوطه جراحی را ببینند. دوربین ویدئو به چشمی لاپاروسکوپ متصل شده و به مکانیسم تمرکز (focus) دستی یا خودکاری مجهزاست که فواصل کانونی متفاوتی را تنظیم می کند. تصویرگرفته شده توسط دوربین به یک دستگاه ضبط ویدئو منتقل شده و جهت پخش تصاویر به یک نمایشگر می رود.
منبع نور
برای انتقال نور به داخل حفره صفاقی یک منبع نوری ضروری است.معمولاً از یک منبع نوری گزنون استفاده می شود که تحت عنوان نور سرد شناخته می شود.این به آن معنا نیست که انتهای طناب نوری نمی تواند بسیار داغ شود بلکه صرفاً نشانه آن است که نور توسط رشته های فیبرنوری منتقل می شود.نباید اجازه تماس بین انتهای طناب نور و پوشش های جراحی (Drapes) یا بدن بیمار داده شود زیرا احتمال بروز سوختگی پوستی وجود دارد.
تروکارها
تروکارها ممکن است از جنس استیل و قابل استفاده مجدد و یا از نوع پلاستیکی و یکبار مصرف باشند (شکل2). تروکارهایی که بطور شایعتر استفاده می شوند بین 12-2 میلی متر هستند.تروکارها بطور تیپیک واجد یک تروکار داخلی تیز ویک پوشش خارجی هستند.نوک تروکار ممکن است مخروطی، هرمی یا مشتمل بر تیغه های تیزجمع شونده پیچیده تری مثل آنچه که در تروکارهای یکبار مصرف وجود دارد،باشند.
ابزارهای جراحی
انواع مختلفی از ابزارهای گرفتن نسج در دسترس است.Graspors با انتهای غیر آسیب رسان را می توان برای ساختمان های ظریفی چون روده و لوله های فالوپ استفاده کرد،درحالی که انواع آسیب رسان (تروماتیک) بطور تیپیک برای خارج کردن نسوج و بیوپسی استفاده می شود (شکل3). قیچی های اندوسکوپیک ممکن است برای برش بطریقه مکانیکی و یا الکتروسرجری استفاده شوند (شکل 4). سوزن گیرها و هل دهنده های گره برای بخیه زدن داخل بدنی و خارج بدنی در دسترس هستند.
شستشودهنده - مکنده (Irrigator-Aspirator)
ممکن است مایعات را بوسیله یک شستشودهنده مکنده بداخل لگن پمپ کرده و سپس خارج کرد.گسترش این سیستمها از یک کانون ساده متصل به یک سرنگ تا سیستم های موتور دار با کارایی بسیار بالا برای جریانهای سریع و پرفشار مایع متغیر است.
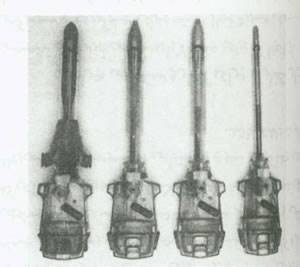
شکل 2: انواع تروکار مورد استفاده در لاپاراسکوپی (از چپ به راست). تروکارهای 5، 11 و12 میلی متری و تروکار 12 میلی متری مورد استفاده در لاپاروسکوپی باز.
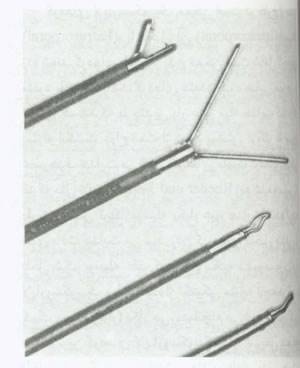
شکل 3:(بالا) فورسپس بیوپسی Semm که برای انجام بیوپسی بافتی و جدا کردن طریف نسوج بکار می رود (دومی از بالا) نگهدارنده (Grasper) روده که برای نگه داشتن و گرفتن روده بدون ایراد آسیب به آن استفاده می شود.(دومی از پایین) فورسپس لوله فالوپ که برای دستکاری و جابجایی بدون آسیب لوله های فالوپ بکار می رود و (پایین) نگه دارنده،غیرآسیب رسان (Artaumatic grasp) که برای دستکاری و جابجایی بدون آسیب نسوج مختلف استفاده می شود.
Staplerها (گیره ها)
در سال 1990 برای نگه داشتن و جدا کردن نسوج استفاده از یک وسیله گرفتن (Stapling) لاپاروسکوپیک بنام Gastrointetinal Anastomosis) Endo- GIA) شروع شد (شکل 5). هنگامی که آرواره های دستگاه روی نسج بستنه شوند و دسته فشرده شود،6 ردیف Stapleهای مرتب شده سه سانتیمتری در محل مستقرشده و همزمان تیغه چاقویی نسج را بریده و سه ردیف staple را در هر طرف برش باقی می گذارد.
گیرنده های عروقی
گیرنده های عروقی آندوسکوپیک ممکن است برای دستیابی به هموستاز درعروق خونریزی دهنده بکار روند (شکل 5). مزیت اینها،امکان استفاده از نزدیکی ساختمان های حیاتی است که در چنین محل هایی استفاده از کوتر می تواند منجر به صدمه حرارتی جانبی شود.این وسایل بویژه درنشت خون از پایه های Endo.GIA مفید هستند.
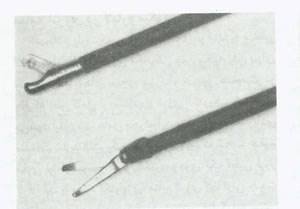
شکل 4:ممکن است از قیچی های جراحی قابل استفاده مجدد،(بالا)با قیچی های یکبار مصرف (پایین )استفاده شود.
ابزارهای دستکاری و جابجایی رحم
تعدادی ازابزارهای جابجایی و دستکاری رحم وجود دارد که ممکن است در رحم یا سرویکس قرار گرفته،با جابجا کردن رحم به جلو،عقب یا طرفین دسترسی بهتر به لگن را فراهم می کند.بسیاری از اینها همچنین توانایی انجام تزریق رنگ بداخل لوله ها به منظوراثبات باز بودن لوله های فالوپ را دارند.

شکل 5:بالا:Endo -GIAبرای نگهداشتن و جدا کردن بافت،و پایین :Endoclipبرای دستیابی به هموستاز.
منابع انرژی در لاپاروسکوپی
اصطلاح پلویسکوپی (Pelviscopy) در ابتدا به منظور اشاره به استفاده از انرژی مکانیکی چون بخیه زدن برای نگه داشتن پایه های نسجی بزرگ و حصول هموستاز درحالیکه بطور کامل استفاده از انرژی الکتریکی خودداری می شود،ابداع شد. عامل محرک این روش بروزتعداد زیادی صدمات شدید الکتریکی در بیمارانی بود که تحت عقیم سازی لوله ای بوسیله روش الکتروسرجری تک قطبی قرار گرفته اند.با بهبود تکنولوژی،منابع انرژی گوناگونی جهت استفاده درجراحی آندوسکوپی در دسترس قرار گرفته است.
انرژی اندومکانیکال
ساده ترین روش بستن بطریقه لاپاروسکوپیک (Ligature)،استفاده از Roeder Loop است که توسط semm برای کاربری لاپاروسکوپیک متناسب و تغییر شکل یافته شده است.این روش بصورت یک گره از قبل بسته شده است که برروی یک میله هل دهنده قرار دارد که برای راندن حلقه بخیه بدور پایه نسجی به منظور هموستاز بکار می رود. (شکل 6). بخیه زدن لاپاروسکوپیک را می توان برای بستن سطوح برهنه صفاقی،ترمیم و انسیزیون های رحمی مربوط به میومکتومی،ترمیم آسیب روده یا مثانه، نگهداشتن پایه های بافتی در هیسترکتومی لاپاروسکوپیک،و انجام یوتروپکسی رتروپوبیک بکاربرد.

شکل 6:بالاSurgiwhipکه بعنوان یک روش از قبل گره خورده جهت بخیه زدن خارج ازبدن بکار می رود .وسط:Endoloopکه برای گرفتن و نگهداشتن یک پایه نسجی هنگامی که نیاز به بخیه زدن نیست بکار می رود .پایین :Endostitchکه برای بخیه زدن نسج با استفاده از یک سوئیچ فشاری(Toggle switch)بکار می رود و نیاز به دستکاری و استفاده از سوزن بخیه را غیر ضروری می سازد.
گره های لاپاروسکوپیک ممکن است درخارج از بدن (Extracorporal)، یا داخل آن (Intracorporal) (بسته)زده شوند.گره های خارج از بدن ممکن است شامل گره های منفرد یا متعدد باشد.گره های متعدد،گره هایی مربعی و لغزشی هستند که با چندین بارعبورمیله هدایت کننده که بمنزله انگشت جراح است از درون پوشش تروکار به سوی عضو هدف هدایت می شوند.گره های منفرد،گره های لغزشی اند که مثل Roeder and Fisherman's زده شده و سپس از طریق پوشش تروکار بوسیله یکبار عبور هدایت کننده گره به سوی بافت هدایت می شود. زدن گره های داخل بدنی در داخل شکم بوسیله حلقه کردن نخ بخیه بدور سوزن گیر لاپاروسکوپیک و با استفاده ازتکنیکی مشابه آنچه در گره با کمک وسیله (ابزار) بکار می رود،انجام می شود.بطورکلی محکم ترین گره های لاپاروسکوپیک گره مربعی مسطح داخل بدنی و گره مربعی لغزشی چند مرحله ای بدنی هستند. تنها گره های یک مرحله ای لغزشی که استحکامی مشابه اینها دارند عبارتند از گره 4-s و گره Fisherman. این گره های محکم در مواردی که نیاز به کشش مداوم بافتی وجود دارد مثل یوتروپکسی رتروپوبیک از طریق لاپاروسکوپی، توصیه می شود.
بخیه زدن بطریقه لاپاروسکوپی نیازمند تجربه قابل توجهی در قرار دادن مطمئن سوزن در سوزن گیر وزدن دقیق و درست بخیه است.برای خاتمه دادن به این مساله Endostitch ابداع شد که در آن سوزن از قبل مستقرشده،و بخیه در نسوجی با ضخامت تا 2 سانتیمتر،با بستن یک دسته ویک Toggle switch، زده می شود. Endostitch ابزاری 10 میلی متری با آرواره هایی به پهنی 4 میلیمتر و طول 2 سانتیمتراست(شکل6).
الکتروسرجری (جراحی با الکتریسیته)
انرژی الکتروسرژیکال را می توان برای خشک کردن و Fulguration نسج بکار برد.بسیاری از مخاطرات جریان الکتریکی تک قطبی با پیشرفت های تکنولوژیکی مثل واحد الکتروسرژیکال عایق شده و پایش جریان برگشتی الکترو (پایش کیفی تماس) بر طرف شده است.بهرحال جراح باید از پدیده های دیگری چون اتصال (Coupling) مستقیم و ظرفیتی و همچنین هدایت حرارتی جانبی بدور از محل الکترود فعال آگاه باشد. اتصال ظرفیتی ممکن است اجازه انتقال 40-5% جریان عبوری را از طریق یک هادی عایق بندی شده یا «متصل» به یک هادی دیگر بدهد.الکترود فعال عایق بندی شده یک ابزار تک قطبی که از طریق مجرای عملی لاپاراسکوپی عبور داده می شود،می تواند تا 40% جریانش را به لاپاروسکوپ منتقل کرده و موجب بروز صدمات پایدارالکتریکی در بافت هایی شود که با لاپاروسکوپ در تماسند.برای کم کردن این خطر می توان از یک پوشش تروکار فلزی به منظور فراهم آوردن یک مسیر کم مقاومت در طی دیواره شکم بطوری که الکتریسیته بتواند بدون ایجاد صدمه به الکترود برگشتی برسد،استفاده کرد.بیشترین خطر ایجاد اتصال ظرفیتی هنگامی رخ می دهد که تروکارهای «هیبرید» بکارمی رود (کانولهای فلزی با قبضه پلاستیکی مربوط به جدارشکم).
فورسپس های دو قطبی با هدایت جریان بین آرواره های فورسپس که به مثانه الکترودهای فعال و برگشتی هستند.عمل می کنند.ازاین رو حوادث مربوط به اتصال بطور کامل بر طرف می شوند.با این حال صدمات حرارتی جانبی در نسوج مجاور الکترود رخ می دهد.درموردی که ظن به آسیب روده کوچک وجود دارد باید انجام مینی لاپاراتومی همراه با برداشتن بخش مورد ظن روده را در نظر داشت.بخاطر اینکه همیشه صدمات الکتریکی از محدوده ضایعه قابل مشاهده فراتر می روند،این صدمات را باید برداشت و هرگز نباید بطور متقاطع دوخته شوند.بعلاوه نباید خطوط Staple را بروش الکتریکی منعقد (electrocogulate) کرد زیرا ممکن است بافت چروکیده و جمع شود که منجر به خونریزی شده،و همچنین staple ممکن است الکتریسیته را در مسیری ناشناخته هدایت و موجب آسیب نسجی شود.
لیزر
واژه لیزر مخفف عبارت انگلیسی «تقویت نور بوسیله انتشار خود بخودی پرتو» است. لیزرهای جراحی که برای کاربردهای ژنیکولوژیک در دسترس هستند عبارتند از Co2، آرگون، پتاسیم، تیتانیل - فسفات (KPT) و نئودایمیوم:ایتریوم - آلومینیوم -یاقوت (Nd-YAG).اینها توانایی تبخیر، برش، و به درجات متغیری انعقاد نسوج را دارند.دراینجا نگرانی در مورد سوختگی متناوب زمینه، اتصال مستقیم یا ظرفیتی، یا تقسیم و انشعاب جریان و مسیر واجد کمترین مقاومت، آنچنانکه در مورد الکتروسرجری هست، وجود ندارد.
مزایا و معایبی برای استفاده از هر نوع طول موج وجود دارد. لیزر Co2 تبخیر نسجی عالی ایجاد کرده و صدمه حرارتی کمی بر جای می گذارد. مایع شستشو دهنده نیز بعنوان یک مانع عالی برای انرژی لیزر Co2 عمل می کند.برای جراحانی که ترجیح می دهند بافتها را با تماس برش دهند،لیزرهای فیبراپتیک قابل استفاده اند، مثل فیبرهای هم محور Nd-YAG که با یک نوع از جنس یاقوت کمبود مصنوعی مجهز شده اند.توانایی نفوذ انرژی خام لیزر Nd-YAG از یک رسته کوارتز عبور داده شود، در داخل نسج تا 4 میلی متر است که باید هنگامی که در نزدیکی حالب یا روده استفاده می شود،مد نظر باشد.با این حال نوک یاقوتی خروج انرژی لیزر را محدود می کند و صدمه بافتی هنگامی که با یاقوت برش داده می شود،معمولاً کمتر از یک میلی متر است.استفاده از لیزر در سالهای اخیر کاهش یافته است،که عمدتاً بدلیل هزینه بالاتر آن و نیز افزایش ایمنی سایر منابع انرژی است.
چاقوی جراحی هارمونیک
چاقوی جراحی هارمونیک با استفاده از لرزش با سرعتی در حد 55000 دور در ثانیه بعنوان منبع انرژی، پیوندهای هیدروژنی بافت ها را شکسته،منجربه برش یا بهم آوردن عروق می شود.چاقوی جراحی هارمونیک بصورت چاقوی نوک گرد 5 یا 10 میلی متر،یا قیچی 10 میلی متر در دسترس می باشد.این روش ممکن است انتقال انرژی حرارتی جانبی کمتری ایجاد کند،و خطر صدمات الکتریکی وجود ندارد.
(استقرار) وضعیت بیمار برای جراحی لاپاروسکوپی
بیمارباید برروی تخت جراحی طوری قرار داده شود که سرین هایش برروی لبه تخت باشد تا امکان قرار دادن و استفاده از وسایل دستکاری و جابجایی داخل رحمی (intrauterine manipulator) باشد. رانهای بیمارباید در همان سطح بدن و شکم باشند نه مثل وضعیت لیتوتومی،تا امکان آزادی حرکت برای قراردادن و استفاده از ابزارهای لاپاروسکوپیک وجود داشته باشد. رکاب ها باید برای
نگه داشتن بخش تحتانی ساق بحد کافی و فراوانی بالشتک گذاری و نرم باشند تا ضمن نگه داشتن ساق پا،ایجاد هیچ گونه فشارنقطه ای ننمایند.استفاده از رکابهایی که بدون نیاز به برداشتن پوشش بیمار (drape) قادربه بالا آمدن هستند،ارجح است،زیرا می توان برای دستیابی راحت تر واژینال از وضعیت لیتوتومی استفاده کرد.
ورود به حفره شکم
ورود به حفره شکمی می تواند در آغاز از طریق ناف و با استفاده از سوزن Veress (شکل7)،گذاشتن مستقیم تروکار،یا بروش لاپاروسکوپی باز،باشد. دو روش اول تکنیک های کور (Blind)جا گذاری هستند در حالیکه در روش لاپاروسکوپی باز،با ایجاد یک برش که حدوداً به اندازه تروکاراست و با استفاده از یک چاقوی جراحی مستقیماً وارد حفره شکمی می شوند.غالباً از این روش هنگامی استفاده می شود که چسبندگی های زیر ناف وجود داشته یا مورد ظن باشند.
هنگامی که از سوزن Veress استفاده می شود،درمحل ناف برش پوستی اولیه ای داده می شود.ناف باید بالا نگه داشته شده و تیغه و چاقو به موازات محور طولی بیماری نگه داشته شود تا از برش غیر مترقبه عروق بزرگ جلوگیری شود.
متخصص بیهوشی با استفاه از کاهش فشار معده و تخلیه آن بوسیله لوله معده خطر ورود اتفاقی سوزن Veress یا تروکار را بداخل معده بیش از حد متسع،کاهش خواهد داد. شکم بیمار باید کاملاً شل باشد تا اجازه بالا نگه داشتن کافی برای قرار دادن سوزن Veress یا تروکار را بدهد.همچنین بیمار باید برروی تخت بصورت صاف قرار داده شود،زیرا اگر ابتدا از وضعیت ترندلنبرگ استفاده شود سوزن ممکن است بیشتر از آنکه به حفره لگنی هدایت شود،به عروق بزرگ نزدیک شود.دربیماران لاغر،سوزن یا تروکار باید با زاویه 45 درجه نسبت به محور قائم هدایت شود تا از عروق بزرگ دور بماند.دربیماران چاق آئورت بطور تیپیک بالاترازسطح ناف قرار داشته و بنابراین سوزن Veress یا تروکار ممکن است تا زمانی که جداره شکم بحد کافی بالا نگه داشته شده باشد،مستقیماً بصورت عمودی و با زاویه 90 درجه نسبت به محور طولی بدن بیمار وارد شود. اگر سوزن Veress بجای آنکه اشتباهاً در فضای پره پریتونئال (پیش صفاقی) وارد شود بطور صحیح بداخل حفره شکم وارد شود، بالا کشیدن جداره قدامی شکم موجب ایجاد فشار منفی می گردد که بر روی insuffator قابل مشاهده است.
هنگامی که دمیدن (insufflation) با جریان کم (سرعت جریان حدوداً یک لیتر در دقیقه) شروع شود،فشارداخل شکمی باید کمتر از 8 میلی متر جیوه بماند.اگر فشار داخل شکمی بیشتر از 8 میلی متر جیوه باشد احتمال دمیدن درفضای خارج صفاقی بالاست،و مسیر دستیابی به حفره شکم باید مجدداً ارزیابی شود.
همچنین می توان از محل های جایگزین برای دمیدن استفاده کرد عبارتند از خط زیر بغل قدامی چپ در ربع فوقانی چپ، بن بست خلفی (دوگلاس)، نمای فوقانی ناف،و حدفاصل بین ناف و سمفیز پوبیس.
قرار دادن تروکار ثانویه
معمولاً برای بیشتر اعمال لاپاروسکوپیک یک یا دو دریچه ثانویه کافی است که ممکن است خارج تر از شریان اپی گاستری تحتانی یا در خط وسط و بالای مثانه قرار داشته باشد.اندازه و تعداد تروکارها به عمل و ابزارهای مورد استفاده بستگی دارد. ممکن است یک تروکار 5-2 میلی متری برای جابجا کردن احشاء لگنی به منظور مشاهده بهتر در لاپاروسکوپی تشخیصی بکار رود.بیشتر ابزارها به اندازه یک دریچه ی 5 میلی متری هستند. درمورد جراحی پیشرفته لاپاروسکوپی،اگرقرار باشد ازیک Endo-GIA استفاده شود،باید یک تروکار 12 میلی متری را مستقرکرد.قرار دادن یک سوزن نمره 22 در دیواره قدامی شکم در محلی که قرار است تروکار وارد و مستقر شود می تواند در تعیین مسیری ایمن بدور از شریان اپی گاستر تحتانی کمک کننده باشد تروکارهای ثانویه باید به طریقه ای کنترل شده و زیر دید مستقیم کار گذاشته شوند.

خارج کردن نسوج
قطعات کوچک بافتی ممکن است از طریق مجرای تروکار 5 میلی متری خارج شوند، در حالیکه برداشتن
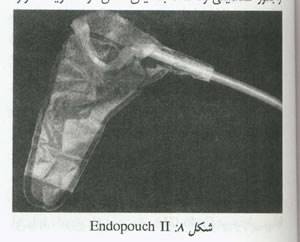
نمونه های متراکم و بزرگی چون میوم می تواند وقت گیر باشد.نمونه های پر از مایع مثل کیست های تخمدانی ممکن است در کیسه های پلاستیکی ویژه خروج نمونه قرار داده شده و سپس درحالیکه داخل کیسه هستند تخلیه (درناژ) شوند تا از پاشیدن و ریختن آن جلوگیری شود (Endocatch و Endopouch II) (شکل 8).بن بست دوگلاس فراهم کننده محلی بزرگ برای خروج نمونه است.کولپوتومی خلفی ممکن است بطریقه واینال یا لاپاروسکوپیک انجام شود،به منظوربالا آوردن بن بست خلفی (کولدوساک) یک قلم اسفنجی مرطوب و لغزان (Lubricated) در فورنیکس خلفی قرار داده شده و با استفاده از لیزر،قیچی های یک قطبی یا چاقوی جراحی هارمونیک برشی بین رباطهای یوتر و ساکرال داده می شود تا به واژن در بالای اسفنج برسد.
بطور جایگزین ممکن است بوسیله یک خرد کننده دستی یا الکترومکانیکی،قطعه قطعه کردن انجام شود.بطورکلی اگر نمونه از لگن جدا شده است،قطعه قطعه کردن نباید بوسیله کوتر تک قطبی انجام شود،چون نمونه تنها هنگامی اتصال الکتریکی خواهد داشت که در تماس با سایر نسوج باشد.
درمان لاپاروسکوپیک توده های آدنکسال
نقش لاپاروسکوپی در ارزیابی و درمان توده های آدنکسال هنوز مورد مناقشه است. مساله در تعیین قبل از عمل اینکه چه توده هایی به احتمال بیشتر خوش خیم هستند، شناسایی و درمان بدخیمی در حین عمل، و دانستن اثرریخته شدن قبل از عمل توده آدنکسال نمی تواند بدخیمی را بطور تضمینی رد کند.با این حال در اکثریت موارد اگر بررسی کافی صورت گرفته باشد ظن قوی وجود خواهد داشت. اگر بدخیمی یافت شود،جراح باید آماده انجام عمل جراحی مناسب به منظور مرحله بندی باشد.
اثر پارگی نئوپلاسم تخمدانی در حین عمل بر پیش آگهی،موضوعی در هم ریخته است. در سال 1973، Webb و همکارانش پیش آگهی بدی را پس از پاشیده شدن تومور گزارش کردند.با این حال با استفاده از تحلیل چند متغیری،اطلاعات جدید این یافته را تایید نمی کند.Dembo و همکارانش 519 بیمار مبتلا به مرحله I سرطان اپی تلیالی تخمدان را مورد مطالعه قرار دادند و دریافتند که تنها عواملی که بر میزان عود موثرند درجه تومور،وجود چسبندگی های متراکم،و حجم بالای آسیت،می باشند. پارگی حین عمل اثر منفی بر پیش آگهی نداشته است. Sainz de la Cuesta و همکارانش پیش آگهی بدی را دربیمارانی که پارگی حین عمل داشتند گزارش کردند اما اعتراف کردند که تفاوت در بقای بیماران ارزش آماری ندارد.
هنگامی که لاپاروسکوپی جهت ارزیابی یک توده آدنکسال انجام می شود باید شستشوی صفاق با استفاده از یک شستشو دهنده - مکنده انجام شود.لگن و بخش فوقانی شکم جهت یافتن هرگونه نشانه ای از متاستاز باید مورد مشاهده قرار گرفته و هردو تخمدان از نظر اختلالات سطحی مورد معاینه قرار گیرند.هدف لاپاروسکوپی رد کردن سرطان،و درمان پاتولوژی خوش خیم آدنکسال بطریقه ای مناسب است.در صورت مواجهه با سرطان بلافاصله باید لاپاراتومی انجام شود.اگر نشانه واضحی از بدخیمی در مشاهده وجود نداشته باشد، باز هم تشخیص بافتی برای رد کردن سرطان ضروری است.هرنمونه ای که در مشاهده کلی بوضوح خوش خیم نباشد باید برای برش منجمد ارسال شود.
تکنیک سالپنگواووفورکتومی
تکنیک های برداشتن آدنکس شامل استفاده از بستن حلقه ای (loop ligature)،بخیه زدن،الکتروکوتریک قطبی و دو قطبی، و Staple است.حالب را باید شناسایی کرد؛ این کار براحتی با مشاهده اطراف محل دو شاخه شدن شریان ایلیاک مشترک انجام می شود.اگرنتوان آن را مستقیماً مشاهده نمود،ممکن است با تشریح و یا با قرار دادن یک stent در آن بطریقه سیستوسکوپی آن را مشخص کرد.رباط اینفاند یبولوپلویک چه با الکتروکوتری و یا stapler گرفته
شود،باید آن را تحت کشش نگهداشت تا از حالب و دیواره های طرفی لگن دور بماند. اگر وسیله stapling بکار رود، یک یا دو بار استفاده از آن می تواند رباط آویزان کننده تخمدان را تشریح (dissect) کند، و یک Endo-GIA منفرد یا انعقاد بوسیله فورسپس دو قطبی برای تکمیل عمل کافی خواهد بود.
آسپیراسیون کیست تخمدانی و سیستکتومی
آسپیراسیون کیست تخمدانی و سیستکتومی متعاقب آن در بیماران یائسه با یافته های کم خطر قبل ازعمل با موفقیت انجام شده است.با این حال دراین گروه عمل سالپنگواووفورکتومی گزینه بهتری است. بخاطراینکه عملکرد تخمدانی متوقف شده است،باید بدخیمی را رد کرد. دربیماران سنین باروری معمولاً برای حفظ عملکرد تخمدان،دربیماران سنین باروری معمولاً برای حفظ عملکرد تخمدان،سیستکتومی تخمدانی انجام می شود.بیشترکیست های خوش خیم تخمدان به راحتی از بافت طبیعی تخمدانی اطرافشان جدا می شوند و صفحه جدا کننده خوبی دارند.
برداشتن کیست های خیلی بزرگ از طریق لاپاروسکوپی ممکن است مشکل باشد،و هنگامی که اندازه آنها به بیش از 10 سانتیمتر می رسد،جراح باید بنا به مصلحت لاپاروسکوپی را در نظر داشته باشد.برای انجام آسپیراسیون کیست و سیستکتومی متعاقب آن، تخمدان باید متحرک باشد. در صورتی که بخواهند اول کیست را آسپیره کنند ممکن است یک سوزن نمره 20 نخاعی را از طریق جداره شکم عبورداده،یا یک کانول 5 میلی متری از طریق مجرای لاپاروسکوپ بکار رود.پس از آسپیراسیون، برشی بر روی کیست تا روی کپسول داده می شود.لبه های دیواره کیست و تخمدان توسط فورسپس های نگهدارنده محکمی گرفته می شود.ازاین کشش و کشش متقابل برای جدا کردن کیست ازتخمدان استفاده می شود.
سپس نمونه بوسیله یکی از روشهایی که در بخش خروج نسج ذکرشده،خارج می شود. اگر سطوح برهنه تخمدان نزدیکی قابل قبول و مناسبی داشته باشند.نیازبه بخیه زدن وجود ندارد.اگراختلاف و فاصله عمده ای وجود داشته و نظر جراح بر لزوم ترمیم تخمدان است،می توان از بخیه 6/0 قابل جذب برای به هم رساندن استروما استفاده کرد. پرهیز از بخیه زدن قشر تخمدان ممکن است احتمال ایجاد چسبندگی را کم کند.
هیسترکتومی واژینال کمک شده توسط لاپاروسکوپی
در نظراست هیسترکتومی واژینال با کمک لاپاروسکوپی (LAVH)،هیسترکتومی شکمی را به یک روش واژینال تبدیل کند، چون مزیت تهاجم کمتر را در بیمارانی که از هر نظردیگری کاندید عمل هیسترکتومی شکمی هستند دارد.
بعضی دلایل انجام LAVH عبارتند از نیاز به انجام جراحی دیگری درحفره شکم مثل رها کردن چسبندگی ها،برداشتن اندومتریوز،یا ارزیابی و برداشت یک توده آدنکسال،اگرچه برداشتن تخمدانها معمولاً می توان بطریقه واژینال انجام داد،استفاده از لاپاروسکوپ ممکن است در بعضی موارد کمک کننده باشد.اگرهیسترکتومی واژینال را بتوان در غیاب یک اندیکاسیون برای هیسترکتومی شکمی انجام داد،این روش انتخابی است و نیاز به کمک لاپاروسکوپی نیست summitt و همکارانش در یک کارآزمایی اتفاقی (Randomized)، نشان دادند که LAVH از نظر بهبودی مزیتی بر هیسترکتومی واژینال نداشته و بطور قابل ملاحظه ای پرهزینه تر است. هیسترکتومی واژینال و LAVH در مقایسه با هیسترکتومی شکمی زمان بهبودی کوتاهتری دارند،گرچه مطالعات مزایایی را در زمینه ترخیص سریعتر بیماران از بیمارستان و زمان بهبودی در LAVH در مقایسه با هیسترکتومی شکمی نشان داده اند،هزینه داخل بیمارستانی همراه با LAVH معمولاً منجر به افزایش هزینه کلی می شود که عمدتاً بدلیل ابزار گذاری گران قیمت اضافی است.
تنوع زیادی در تکنیک های LAVH وجود دارد که از یک مشاهده ساده حفره صفاقی و سپس انجام هیسترکتومی واژینال،تا انجام یک هیسترکتومی کاملاً لاپاروسکوپیک بدون رویکرد واژینال متغیر است.بطور شایعتری لاپاروسکوپ برای کمک به برداشتن آدنکس یا جدا کردن بخش فوقانی رحم تا سطح بلافاصله بالا یا پایین شریان رحمی،بکار می رود.
هنگامی که از stapleهای Endo-GIA استفاده می شود، دو دریچه جانبی 12 میلی متری علاوه بر دریچه نافی تعبیه می شود. برای برداشتن تخمدانها ابتدا باید حالب در پشت صفاق شناسایی و مشخص کرد،یا ممکن است آن را با تشریح یافت.سپس Endo-GIA در عرض رباط
اینفاندیبولوپلوپک قرار داده می شود.قبل از شلیک Staple برای اطمینان از عدم درگیری اعضاء حیاتی،باید دو سوی Endo-GIA را مشاهده کرد.ممکن است از Endo-GIA اضافی تا رسیدن به سطح شریان رحمی استفاده کرد.بدلیل اینکه Endo-GIA یک سانتیمتر پهنا دارد دوری گزیدن از شریان رحمی توصیه شده است. در بعضی موارد فاصله نزدیکی بین شریان رحمی و حالب وجود دارد،و خط Staple حاصل از Endo-GIA همیشه هموستاتیک نیست و ممکن است نیازمند گیره های عروقی اضافی در نزدیکی حالب باشد، صفاق مثانه ممکن است توسط قیچی های لاپاروسکوپیک جدا شود،سپس وضعیت بیمار به شکل لیتوتومی برای انجام بخش واژینال تغییر می یابد.درانتهای عمل،باید حفره لگنی را برای اطمینان از هموستاز مشاهده کرد. نهایتاً به منظورجلوگیری از عارضه فتق دریچه های جانبی 12 میلی متری در سطح فاسیا بسته می شود.
درد لگنی و نقش لاپاروسکوپی
شایعترین اندیکاسیون و گزارش شده لاپاروسکوپی،درد لگنی است.Pent تنها در 53% بیماران مبتلا به درد مزمن لگنی، پاتولوژی یافت، و Laundberg و همکارانش در 60% موارد پاتولوژی یافتند. در یک بررسی به سال 1993، Howard نقش لاپاروسکوپی را در تشخیص و درمان درد مزمن لگن آزمود.او دریافت که علیرغم استفاده شایع، کمتر از 50% از بیماران پس از لاپاروسکوپی بهبود می یابند.بطور واضح لاپاروسکوپی مشکل تشخیص و درمان درد مزمن لگنی را حل نکرده است.
آندومتریوز
اگر چه اندومتریوز بصورت نقاط آبی تیره «باروت سوخته» توصیف شده است، ممکن است همچنین بصورت ضایعات سیاه، سفید،قرمز،قهوه ای مایل به زرد، و شفاف باشد.برای مشاهده بهتر این ضایعات،باید ضمن ایجاد وضعیت ترندلنبرگ و بکار بردن ابزار جابجایی رحم از دو دریچه یا بیشتر استفاده کرد. اگر تنها یافته آندومتریوز ضایعات تیپیک یا ظریف و جزیی باشد،باید انجام بیوپسی جهت تشخیص بافتی مد نظر باشد.
آیا لاپاروسکوپی در درمان محافظه کارانه آندومتریوز شدید بر لاپاروتومی ارجح است؟در مروری بر 14 مطالعه که از لاپاراتومی بعنوان روش محافظه کارانه درمان آندومتریوز شدید استفاده شده و نیز 15 مطالعه که درمان بوسیله جراحی لاپاروسکوپیک انجام شده (جدول 1) این نتیجه حاصل شد که هنوز اطلاعات کافی برای مقایسه قابل اعتماد بین نتایج لاپاراتومی و لاپاروسکوپی از نظر موربیدیتی،میزان حاملگی،برطرف شدن درد و عود،وجود ندارد،درمان لاپاروسکوپیک آندومتریوز شدید نباید ملایم باشد.برداشتن آندومتریوز ارتشاح یافته درکولدوساک گزارش شده است،اما باید توسط جراحان آندوسکوپیک ماهر انجام شود.
عصب زدایی (Denevation) لاپاراسکوپیک
بعنوان شاهدی بر تاثیر نورکتومی پره ساکرال،اغلب به گزارش Tjaden و همکارانش اشاره می شود.این مولفین گزاش کرده بودند که در 4 بیماری که بطور تصادفی برای لاپاراتومی به همراه برداشتن آندومتریوز و نورکتومی پره ساکرال انتخاب شده بودند درد میانی (خط وسط) بر طرف شده،درحالی که هیچ یک از 4 بیماری که تنها برداشتن آندومتریوز داشتند بهبود نیافتند.متأسفانه این تحقیق بوسیله Institutional Review Board که اعلام کرده بودند این یافته های اولیه ارائه دهنده آن است که دور نگهداشتن بیماران از فوائد نورکتومی پره ساکرال غیر اخلاقی است در آن مرحله متوقف شد.
11 مورد از 13 بیمار بعدی که بصورت غیر تصادفی انتخاب شده بودند و برایشان نورکتومی پره ساکرال انجام شده بود بهبودی را تجربه کردند.هیچیک از 9 بیماری که نورکتومی پره ساکرال نشده بودند بهبود نیافتند.مواردی با میزان موفقیت 97-70% گزارش شده است.چند مورد کارآزمایی آینده نگر تصادفی نیز گزارش شده است.طی یک گزارش توسط Candini و همکارانش در مورد 71بیمار، نشان داده شد که کاهش قابل توجهی در جزء میانی درد قاعدگی ایجاد شده ولی تفاوت آماری قابل توجهی در شیوع و شدت دیسمنوره،درد لگن،و دیس پارونیا وجود ندارد،نورکتومی پره ساکرال از طریق لاپاروسکوپی پیشرفته آموزش دیده و با این عمل آشنایی کافی دارند انجام شود.این عمل عصب زدایی باید برای بیمارانی در نظر گرفته شود که دارای دیسمنوره قابل ملاحظه و مقاوم به درمانهای محافظه کارانه مناسب باشند.
جدول 1:جراحی محافظه کارانه در برابر درمان صبر و انتظار در آندومتریوز
|
0/0 95 CI (
|
|
|
2/2(4و2/1)
4/0(6/1 و10 /0)
9/3(4/9و6/1)
9/27(497 و6/1)
|
تمام بیماران
اندومتریوز خفیف
اندومتریوز متوسط
آندومتریوز شدید
|
مطالعات مشاهده ای در مورد عصب زدایی یوتروساکرال بروش لاپاروسکوپیک (LUNA) که در زمان درمان لاپاروسکوپیک آندومتریوز انجام شده است با 92-72% احساس بهبودی دیسمنوره،نشان دهنده میزان توفیقی مشابه با آن دسته از بیماران است که تنها تحت درمان آندومتریوز قرار گرفته اند.بنظر می رسد عمل LUNA تنها بهبودی نسبی و گذرایی در درد لگنی ایجاد کرده و همراه با عوارض جدی است، بنابراین این روش بجز در شرایط غیر معمول (فوق العاده) توصیه نمی شود.
عقیم سازی لوله ای
روشهای متعددی برای عقیم سازی لوله ای به روش لاپاروسکوپیک برای هر بخش خاص از لوله طراحی شده است.دانستن این روشها و بخش لوله ای مرتبط با آن بسیار مهم است،زیرا با انحراف از روشهای استاندارد با میزان شکست بالاتری همراه است.دراغلب عقیم سازی هایی که امروزه با الکتروکوترانجام می شود،از وسایل دو قطبی بیشتر از تک قطبی استفاده می شود.(شکل9).
اصول کلیدی در الکتروکوتری دو قطبی عبارتند از استفاده از اجزای الکتروسرژیکال متناسب،گرفتن بخش میانی لوله در قسمت مقعر فورسپس کوتر به نحوی که انبر منقار اردکی عروق مشروب کننده که ازدرون مزوسالپنکس عبور می کنند را کوتریزه کند،کواگولاسیون سه ناحیه مجاور هم با انرژی 25 وات(حداقل 3cm) تا هنگامی که آمپرسنج قطع جریان را اثبات کند،دوری گزیدن از ناحیه شاخی لوله (Cornual region) (که واجد عروق بیشتر بوده و احتمال بروز فیستول بیشتری دارد)،و پرهیز از تماس با هر بافت دیگری است.
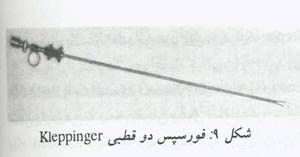
گره پلاستیکی تقویت شده با فنر Hulka-Clemmens را باید 2 الی 3 سانتی متر دیستال به محل اتصال رحم ولوله فالوپ،با زاویه 90 درجه با قسمت تنگه ای (Isthmic)آن و بصورت عمود بکار برد. پس از اینکه گیره قرار داده شد،باید لوله را برای اطمینان از اینکه گیره تمامی لوله را پوشانده مورد معاینه قرار داد. اگر گیره به درستی مستقر نشده باشد، ممکن است گیره دومی گذاشته شود.امروزه با تأیید اخیر FDA،گیره تیتانیومی با پوشش سیلیکون در دسترس است.گیره Filshie در محل تنگی پروگزیمال لوله در 2 تا 3 سانتی متری شاخ رحم بصورت قائم قرار داده می شود. برای اطمینان از اینکه لوله کاملاً پوشیده شده است باید بخش فلزی اپلیکاتور از وراء مزوسالپنکس مشاهده شود.این روشها این مزیت را دارند که در بیمارانی که مایل به آناستوموز لوله ای هستند تخریب کمتری در لوله ایجاد می کند.حلقه فالوپ برروی ناحیه آمپرلر لوله فالوپ قرار می گیرد. لوله گرفته شد و بداخل سیلندر اپلیکاتور کشیده می شود.اپلیکاتور را باید برای کم کردن هرگونه کشش که ممکن است به خونریزی بیانجامد به لوله نزدیک کرد.پس از کارگذاشتن حلقه لوله،بخش حلقه ای و دسته شده لوله باید 2-1 سانتی بوده و دور مجرای لوله ای کامل داشته باشد.
توسط انجمن منتقدین عقیم سازی (CREST) در امریکا،مطالعه آینده نگر Cohort در 9 مرکز طبی انجام شد که طی آن 10685 زن به مدت 8 تا 14 سال پیگیری شده بودند، مشخص شد که میزان شکست بسیاری از روشهای عقیم سازی لوله ای بیش از آن چیزی است که مورد انتظار بوده است.این مطالعه نشان داد که طی 5 سال پس ازعقیم سازی، 1% زنان حامله خواهند شد.کمترین احتمال حاملگی طی 10 سال،پس از روشهای سالپنژکتومی پارسیل پس از زایمان و کوآگولاسیون یک قطبی دیده می شود.بیشترین میزان شکست 10 ساله، درروش گیره Hulka-Clemmens گزارش شده است (36/5 در هر 1000 عمل).
حاملگی نابجا
گرچه درمان لاپاروسکوپیک حاملگی نابجا بینش از سایراعمال لاپاروسکوپیک مورد مطالعه قرار گرفته است.
بیشتر شواهد مساعدی که درمان لاپاروسکوپی حاملگی نابجا را مورد تأیید و تقویت قرار داده اند، حاصل مطالعات توصیفی،موردی-شاهدی، و Cohort بوده است.یک RCT (کارآزمایی کنترل شده تصادفی) با 60 بیمار (30 نفر در هرگروه) که در آن لاپاراتومی با لاپاروسکوپی مقایسه شده،مدت زمان باقی ماندن کمتر و میزان بهبودی سریعتر را در گروهی که به روش لاپاروسکوپیک درمان شده بودند، نشان داد.با این حال برای نشان دادن 50% کاهش در موربیدیتی (ناتوانی) (با 0/05>P) ویک Power 80 درصدی ، 948بیمار مورد نیاز خواهد بود.
تکنیک سالپنژکتومی خطی برای حاملگی نابجا
برای به حداقل رساندن خونریزی،ممکن است 5cc محلول رقیق شده وازوپرسین (20 واحد در 100 میلی لیترسالین) را توسط یک سوزن نمره 21 نخاعی یا سوزن لاپاروسکوپیک بداخل مزوسالپنکس درزیر حاملگی نابجا و نیز بر روی سطح آنتی مزانتریک لوله تزریق کرد. سپس با یک میکروالکترود یا لیزر برشی 1 تا 2 سانتی متری برروی سطح آنتی مزانتریک و در نازک ترین بخش لوله برآمده شده ایجاد می شود.درحالی که برش از طریق دریچه طرف مقابل در حال انجام است،با کشیدن ملایم توسط یک فورسپس غیر آسیب رسان (artaumatic) می توان به بهترین وجه به لوله فالوپ وارد شد. محصولات نابجا معمولاً به راحتی و بوسیله تشریح با آب (Hydrodissection) از جای خود خارج می شوند یا ممکن است توسط فورسپس های لاپاروسکوپیک برداشته شوند.اگردرمحل لانه گزینی خونریزی تداوم یابد،باید توسط یک فورسپس ظریف دو قطبی (microbipllar)،الکترود سوزنی، یا پرتو غیرمتمرکز لیزر به ملایمت کوتریزه شود.
میومکتومی لاپاروسکوپیک
میومکتومی لاپاروسکوپیک بدلیل اینکه برای بخیه زدن مناسب نقص حاصله در رحم نیازبه مهارت تخصصی دارد یکی ازاعمال جراحی مشکل توسط لاپاروسکوپی قلمداد می شود.هیچ کنتراندیکاسیون مطلقی از نظر اندازه میوم برای روش لاپاروسکوپی وجود ندارد،زیرا نتایج عمل تا حد زیادی به انجام دهنده آن بستگی دارد.برداشتن فیبروئیدهای بزرگ پایه دار (8 تا 10 سانتیمتری) کاملاً آسان است اما ممکن است برای قطعه قطعه کردن شان بطریقه دستی وقت زیادی صرف شود.ازسوی دیگر،برداشتن فیبروئیدهای بزرگ داخل جداری ممکن است حتی توسط متخصصین جراحی لاپاروسکوپی 4 ساعت طول بکشد. بیشتر گزارشات میومکتومی لاپاروسکوپیک محدود به مواردی هستند که با روش باز مقایسه نشده اند علاوه بر آن در این دسته مطالعات درمان فیبروئیدهای بزرگ داخل جداری که برداشتن شان می تواند کاملاً کسالت آورباشد،جدا نشده است. اخیراً Stringer و همکارانش تجارب شان در مورد میومکتومی باز (به تعداد 49 مورد بین 1995-1983) و میومکتومی لاپاروسکوپیک (49 مورد بین 1995-1993) را بصورت گذشته نگر مقایسه کردند.میانگین مدت حضور در اطاق عمل در گروه لاپاروسکوپیک بطور قابل توجهی بیشتر بود،با این وجود،میانگین روزهای حضور در بیمارستان،میانگین میزان خون از دست رفته،و عوارض پس از عمل به طور قابل توجهی در گروه لاپاروسکوپیک کمتر بود.تفاوت آماری در هزینه ها وجود نداشت.اندازه رحم در گروه هایی که تحت عمل باز قرار گرفته بودند 12 تا 14 هفته، و در مقابل در گروه لاپاروسکوپیک 11-9 هفته بود.تا امروز اطلاعاتی کافی مبنی بر اثرات دراز مدت این گونه ترمیم ها بر حاملگی بعدی در دست نیست.
آویختن سرویکس (Culposuspension) به روش لاپاروسکوپیک
تا امروز،بیشتر اطلاعات مربوط به کارآیی و ایمنی یوتروپکسی لاپاروسکوپیک از مواری بدست آمده که پیگیری محدودی داشته اند. هیچ گونه اطلاعاتی راجع به پیگیری 5 ساله برای مقایسه این روش با روشهای باز متداول وجود ندارد. در سال 1993،Liu نتایج 58 مورد از یوتروپکسی Burch تعدیل شده برای لاپاروسکوپی را گزارش کرد.میزان موفقیت او در پیگیری 6 تا 22 ماهه،95% بود.میانگین حضور دراطاق عمل (غیر ازاعمال جراحی لاپاروسکوپیک و واژینال همراه)، 73 دقیقه با میزان خون از دست رفته تخمینی در حد 50 میلی لیتر بود. میانگین حضور در بیمارستان 1/2 روز بود،و در 2 بیمار آسیب به مثانه ایجاد شده بود (8/5%).در سیر بیمار تشخیص ناپایداری دترسور (Detrusor Instability) پس از عمل گذاشته شد که به
خوبی به درمان طبی پاسخ داد.
Liu،گروهش را تا 1994 اضافه کرد تا به مجموع 132 بیمار رسید که 127(96%) بیمار از جراحی راضی بودند.در زمان جمع آوری اطلاعات (آگوست 1993) 55 بیمار به مدت 1تا 2 سال پیگیری شده بودند،اما تنها 10 بیمار برای مدت بیش از 2 سال تحت پیگیری بودند.این اطلاعات پیشنهاد دهنده آن است که در دستان یک جراح لاپاروسکوپیک با تجربه،نتایج بالینی کوتاه مدت عمل لاپاروسکوپیک Burch کاملاً خوب است.
Polascik و همکارانش 22 بیمار را که تحت یوتروپکسی متداول (12مورد)و Burch (10 مورد) قرار گرفته بودند را بصورت مطالعه ای موردی شاهدی گزارش کردند. درگروه لاپاروسکوپیک به ازای میانگین پیگیری حدود 20/8 ماه 10 نفر از نظر بی اختیاری حاصل از فشاری (stress incontinence) بطور موفقیت آمیزی درمان شدند.از10 نفر بیمار گروه عمل باز،تنها 7 نفر (70%) بهبود یافتند که میانگین پیگیری در حد 35/6 ماه داشتند.انجام روش لاپاروسکوپیک در حد 35/6 ماه داشتند.انجام روش لاپاروسکوپیک بطور متوسط 1/5 ساعت بیشتر طول کشیده (0/01>P) اما به ضد درد کمتری پس از عمل نیاز داشتند (0/01>P) و بطور قابل توجهی مانده در بیمارستان کاهش یافته بود (1/9 روز در مقابل 4/9روز).اگرچه بنظر می رسد این نتایج مشوق انجام عمل لاپاروسکوپیک Burch باشد، میانگین مدت پیگیری بین دو گروه کاملاً غیر مشابه و اندازه نمونه برای استخراج نتایج قطعی از نظر اثر بخشی خیلی کم است.
Burton در سال 1994 در International Continence Society اطلاعاتی را از یک کارآزمایی تصادفی بالینی با 60 زن ارائه داد که این دو تکنیک را مقایسه می کرد. میانگین تعداد دفعات نشت ادرار در 24 ساعت در گروهی که تحت عمل باز قرار گرفته بودند، 2 بار و در گروه لاپاروسکوپیک 6 بار بود (0/05>P).درحال حاضر برای مقایسه بهتر این دو روش حداقل یک کارآزمایی بالینی تصادفی درچند مرکز در حال انجام است.
لاپاروسکوپی در مطب و میکرولاپاروسکوپی
لاپاروسکوپی درمطب بیانگر استفاده از لاپاروسکوپی در شرایط غیر بیمارستان، با استفاده از آرام بخش در حین هشیاری بیمار (Conscious Sedation) (آرامبخشی داخل وریدی) و بی حسی موضعی بدون همراهی یک متخصص بیهوشی است. میکرولاپاروسکوپی بیانگر استفاده از ابزار گذاری 3-2 میلی متری است، اما ممکن است با استفاده از آرامبخشی در حین هوشیاری یا بیهوشی عمومی انجام شود بی حسی موضعی و آرامبخشی در حین هشیاری از مدتها قبل برای بستن لوله ها (T.L) استفاده می شد. استفاده از ابزارهای میکرولاپاروسکوپی به انجام لاپاروسکوپی در وضعیت آرامبخشی حین هشیاری در مطب به منظور تعیین جزء به جزء علت درد (Pain mapping) در بیماران مبتلا به درد لگنی، مزمن، کمک کرده است. این کار ممکن است در بیماران مبتلا به درد مزمن لگنی با علت نامشخصی مفید باشد، زیرا بیمار را قادر می سازد تا در بررسی لگن، هنگامی که کانون دردناک جستجو می شود، مشارکت کند. بخاطر اینکه این روش نسبتاً جدید است،اثرات تعیین جزء به جزء علت درد از نظر نتایج بلند مدت بررسی نشده است.
هیستروسکوپی
هیستروسکوپی اولین بار توسط Pantaleoni با استفاده از سیستوسکوپی تطبیق داده شده انجام شد. همچنانکه عدسیها و منابع نوری متکامل می شوند، هیستروسکوپ برای نشاندادن حفره آندومتر و دهانه لوله های رحم بکار گرفته شد. برای برداشتن میوم های زیر مخاطی، برداشتن دیواره ها و چسبندگی های (synechia) رحمی،عقیم سازی، کانالیزه کردن و مشاهده لوله های فالوپ و از بین بردن (ablation) آندومتر در درمان DUB استفاده می شود.امرزوه بطور رایج از هیستروسکوپی به همراه دیلاتاسیون و کورتاژ،جهت پرهیز از انجام یک اقدام کورکورانه،استفاده می شود.
قرار دادن ابزار (ابزارگذاری)
هیستروسکوپهای خشک و قابل انعطاف را بر اساس سیستوسکوپ ها و آندوسکوپ های گوارشی ساخته اند.بسته به استفاده از آنها برای مقاصد تشخیصی یا جراحی، قطر خارجی آنها بین 2-10 میلی متر متغیر است. هیستروسکوپ های خشک (Rigid) تشخیصی از دو قطعه،تلسکوپ و پوشش خارجی،تشکیل می شوند.انواع تلسکوپ هیستروسکوپی خشک، با زاویه دید بین صفر تا 70 درجه در
دسترس هستند.پوشش خارجی برای تزریق یک ماده متسع کننده بکار می رود هیستروسکوپ جراحی از سه جزء تشکیل شده است: تلسکوپ جزء عمل کننده،و پوشش خارجی (شکل 10).
جزء عمل کننده قابلیت جای دادن یک الکترود غلتکی،حلقه ای،یا تبخیرکننده را دارد (شکل 11).ممکن است نیروی این اجزاء توسط الکتریسیته تامین شود،این تجهیزات،ابزارهایی تک قطبی محسوب می شوند.همچنین ممکن است لیزرهای آرگون، Nd-YAg، و KTP نیز از درون کانال جراحی (جزءعمل کننده) عبور داده شوند. علاوه بر آن ابزارهای دیگری چون Grasperها و قیچی ها،که نیاز به الکتریسته ندارند را نیز می توان از درون کانال جراحی عبور داد.همچنین منبع نور نیز مورد نیاز بوده و نمایشگر ویدئو در دسترس است. مجاری جداگانه ای برای جریانه های ورودی و خروجی در دسترس است،لذا می توان مایع را به صورت مداوم و به منظور دید بهتر تعویض کرد. شکل 11:(بالا)الکترود حلقه ای مستقیم برای جدا کردن چسبندگی ها و دیواره های رحمی،(وسط)الکترود غلتکی برای تراشیدن و از میان بردن اندومتر بکار می رود .(پایین)الکترود حلقه ای خمیده که برای برداشتن میوم یا اندومتر بکار می رود.
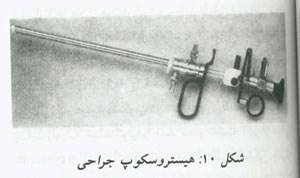
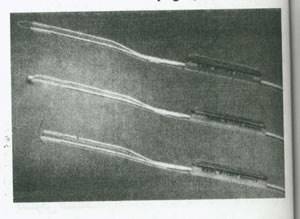
درمقابل هیستروسکوپ خشک چند پوششی، هیستروسکوپ انعطاف پذیر تنها واجد یک جزء قابل هدایت است.انتهای دیستال قابلیت برگشتن 130 الی 160 درجه را دارد. قطر خارجی آن معمولاً بین 3/5 تا 5 میلی متر بوده و یک کانال یک میلی متری برای تزریق ماده متسع کننده دارد.
ماده متسع کننده
استفاده از یک ماده متسع کننده،حفره رحم را از یک فضای بالقوه تبدیل به فضایی می کند که ارائه دهنده منظره وسیعی (همه جانبه ای)ازآندومتراست.بسته به سلیقه جراح و شرایط عمل چندین ماده در دسترس است.برای هیستروسکوپی تشخیصی در مطب که معمولاً مدت کوتاهی طول می کشد،مشخصاً از دی اکسید کربن، نرمال سالین، یا رینگرلاکتات استفاده می شود.ازمحلولهای غیر الکترولیتی اغلب برای موارد جراحی که در اطاق عمل صورت می گیرد،استفاده می گردد.
گاز
مزیت دی اکسید کربن ایجاد انتشار کمتر بدون وجود مایع برای تجمع است و دید و ایمنی عالی فراهم می کند.استفاده از دستگاه دمنده هیستروسکوپی (بجای نوع لاپاروسکوپیک) که فشارآن روی 100 میلی متر جیوه و سرعت جریان کمتر از 100 میلی لیتر در دقیقه به منظور جلوگیری از عارضه آمبولی دی اکسید کربن است، از اهمیت خاصی برخورداراست.معایب دی اکسید کربن شامل تجمع حباب های گاز و خونریزی است که ممکن است دید را مختل نماید.همچنین استفاده از دی اکسید کربن برای کاربرد لیزر Nd-YAG ناسازگار است.
محلول های الکترولیتی با ویسکوزیته پایین
نرمال سالین و رینگر لاکتات بطور معمول جهت مقاصد تشخیصی بکار می روند. مزیت آنها ارزانی و سهولت دسترسی است.با این وجود چون حاوی الکترولیت هستند نباید به همراه الکترودهای تک قطبی بکار روند.اخیراً سیستمی برای استفاده از الکتریسیته همراه با نرمال سالین طراحی شده که ورقه قابل اتصالی دارد که بعنوان الکترود برگشت عمل می کند.این وسیله به امید کاهش خطر
هیپرناترمی ساخته شده است.
محلول های غیرالکترولیتی با ویسکوزیته پایین
معمولاً گلیسین 1/5% و سوربیتول 3% هستند و قابلیت استفاده ایمن ازالکتریسیته را دارند بهرحال چون اینها محلول هایی هیپوتونیک (کم غلظت) هستند،خطر ایجاد هیپوناترمی را به همراه دارند.آنها به سهولت با خون مخلوط می شوند که در مواجهه با خونریزی می تواند مختل کننده دید باشد.بعلاوه هنگامی که گلیسین بداخل گردش خون جذب شود،به آمونیوم و نهایتاً اوره متابولیزه می شود.ممکن است بیماران با اختلال عملکرد کبدی در معرض خطر مسمومیت با آمونیاک و بیماران با اختلال کلیوی در خطر مسمومیت با اوره قرار گیرند.شایعترین مشکل،ادم ریوی است.
محلول های با ویسکوزیته بالا
Hyskon(محلول 32% دکستران 70 در دکستروز) یک محلول غیرالکترولیتی است که با خون مخلوط نمی شود.به این دلیل واجد کیفیت دید عالی و قابلیت استفاده از الکتریسیته است.معایب آن احتمال آلوده کردن وسایل و مدت زمان طولانی جهت پاک شدن آن است.اگرهیستروسکوپ بقدر کافی پاک نشود،ممکن است مجرای آن با سفت شدن Hyskon، مسدود شود.ازآنجا که Hyskon افزاینده حجم پلاسما درحد قابل توجهی است.جذب داخل عروقی آن می تواند به عوارض جدی هیپوناترمی بیانجامد،خصوصیات اسموتیک Hyskon حجم پلاسما را به نسبت 1 به 8 افزایش می دهد. Hyskon همچنین بر پلاکتها، فاکتور بیماری فون ویلبراند را تقلید کند. واکنشهای آنافیلاکتوئید نادراما قابل توجهی نیز گزارش شده است.به منظورجلوگیری از افزایش حجم مایعات (اضافه بار مایع) اعمال جراحی را باید با استفاده از مقادیر 100 تا 500 میلی متر انجام داد.
هیستروسکوپی تشخیص
هنگامی که از یک هیستروسکوپ تشخیصی کوچک استفاده می شود بندرت نیاز به دیلاتاسیون سرویکس هست. قبل ازقرار دادن هیستروسکوپ باید برای ارزیابی محور سرویکس و رحم به منظورجلوگیری از سوراخ شدن،معاینه دو دستی انجام شود. برای مستقیم کردن مجرای سرویکس،با تناکولوم تک دندانه ای به قدامی سرویکس گرفته می شود.در حالی که هیستروسکوپ در دهانه سرویکس قرار می گیرد .باید زوایه تلسکوپ را مد نظرداشت. اگر ازنمای Foreoblique استفاده می شود،نما (منظره)اندکی جلوترخواهد بود.همچنانکه هیستروسکوپ زیر دید مستقیم به پیش رانده می شود،کانال آندوسرویکس ارزیابی می گردد.وقتی حفره رحم متسع شود نمای وسیعی از حفره آندومتر بدست می آید.باید هر منطقه غیر طبیعی حفره اندومتررا ارزیابی و بررسی کرد.همچنین بررسی دهانه لوله ها نیز الزامی است.کل معاینه به زمانی بیش از چند دقیقه نیاز ندارد.
هیستروسکوپی جراحی
هیستروسکوپی به منظور جراحی در قبال یک اختلال شناخته شده انجام می شود و برای اینکه اجازه عبور هیستروسکوپ بزرگتر را بدهد که بطور تیپیک قطر خارجی 8 میلی متر دارد، معمولاً نیازمند دیلاتاسیون سرویکس است.قبل ازعمل ، استفاده از گشادکننده های غیرفعال سرویکس مثل لامیناریا درآماده سازی سرویکس مفید بوده،خطر سوراخ شدن رحم را کاهش می دهد.ماده ای باید انتخاب شود که با ابزار جراحی مورد استفاده سازگار باشد.برای جلوگیری از ایجاد ناخواسته سندرم اضافه بار مایع، باید میزان ورودی و خروجی مایع پایش شود.درمورد کیسه های 3 لیتری که اغلب در هیستروسکوپی جراحی بکار می روند،در صورتی که از روش چشمی (مشاهده ای) برای تخمین ورودی و خروجی استفاده شود،چون ممکن است حاوی مقادیرمتغیری از مایع باشند ممکن است محاسبه را دچار مشکل سازد. امروزه سیستم هایی که بر اساس وزن لحظه به لحظه مایع برای تعیین تعادل مایع عمل می کنند،با دقتی قابل توجه در دسترس هستند.
لیومیوم
بیمارانی که دارای لیومیوم زیر مخاطی علامت دار هستند،کاندید عمل برداشت به روش هیستروسکوپی می باشند.استفاده از یک آگونیست GnRH به مدت 2 ماه
قبل ازعمل به بیمار فرصتی برای افزایش هماتوکریت داده و ممکن است حجم رحم را 30 تا 50% کم کند.بطورشایع از الکترود حلقه ای برای تراشیدن میوم های هم سطح رحم استفاده می شود.ممکن است از جریان 100 تا 120 وات برای بریدن یا منعقد کردن استفاده شود.حلقه را باید به سمت بخش سری میوم پیش راند و برش با کشیدن حلقه به طرف اپراتور انجام می شود.در مورد فیبروئیدهای پایه دار نباید ساقه را تا پایان جراحی قطع کرد زیرا آویختگی آن از جداره رحم،انجام عمل را ساده تر می کند. هنگامی که قطعات متعددی از میوم جمع شده موجب اختلال در دید می گردند، هیستروسکوپ به عقب کشیده شده،از فورسپس های پولیپ برای برداشتن قطعات استفاده می شود. VaporTrode برای تبخیر میوم ها طراحی شده و لذا ضرورت برداشتن قطعات میوم را منتفی می سازد.
VaporTrode از جریان برشی خاص با قدرت 200-160وات استفاده می کند. بدلیل اینکه بندرت تومور بدخیم وجود دارد توصیه شده که قسمتی از تومور بریده شده و جهت تایید بافت شناسی ارسال شود. هنوز برای دانستن اینکه این که این تکنولوژی جدید با تکنیک های برشی چگونه مقایسه خواهد شد،بسیار زود است.
رحم دیواره دار
هیچ ملاک و معیارمشخص و جامعی برای متروپلاستی وجود ندارد.بطورکلی،این کار هنگامی انجام می شود که سابقه نتایج بد حاملگی در یک بیمار مرتبط با یک دیواره رحمی پنداشته شود.اندیکاسیون ها ممکن است شامل سقط های مکرر سه ماهه اول، سقط درسه ماهه دوم،یا سابقه تولد نوزاد نارس می باشند.برای درمان رحم دیواره دار می توان برداشتن دیواره به روش هیستروسکوپیک را با نتایج عالی و عوارض کمتر و به منظور هزینه کمتر نسبت به روش معمول شکمی انجام داد.
برنامه ریزی عمل در اوایل مرحله فولیکولی بخاطر نازکی نسبی پوشش اندومتر به ایجاد دید بهتر کمک می کند. پروفیلاکسی با آنتی بیوتیک توسط بعضی مولفین توصیه شده است.برای برداشتن دیواره،حلقه مستقیم نسبت به حلقه خمیده 90 درجه ارجحیت دارد.اگرالکترود حلقه ای بکار می رود باید از یک محلول غیر الکترولیتی (سوربیتول یا گلیسین) استفاده کرد. همچنانکه الکترود از درون دیواره عبور می کند،آن را باید در مرکز دو دیواره قرار داد.ازآنجایی که بافت عقب رفته و هم سطح حفره آندومتر خواهد شد،همزمان باید بطریقه لاپاروسکوپیک نیز مشاهده صورت گیرد تا از سوراخ شدن رحم جلوگیری شود.دریک گروه 91 نفره از بیمارانی که بدلیل یک یا چند سقط یا ختم حاملگی در اواخر سه ماهه دوم تحت متروپلاستی هیستروسکوپیک قرار گرفته بودند، میزان تولدهای زنده ای در حد 85% بدست آمده است.بعضی جراحان پس از برداشتن دیواره برای ایجاد پوشش اندومتر بر روی ناحیه برداشته شده و به امید جلوگیری از چسبندگی های رحمی،استروژن شده و به امید جلوگیری از چسبندگی های رحمی، استروژن تجویز می کنند.یک مطالعه آینده نگر تصادفی کور (Blinded) نشان داده که تجویزاستروژن پس از برداشتن دیواره سودی ندارد.
خونریزی رحمی بدلیل اختلال عملکرد (DUB): برداشتن یا Ablation آندومتر
لیزر Nd-YAG در ابتدا برای از بین بردن (Ablation) آندومتربکار رفت. پس از آن روشهای الکتروسرژیکال شامل الکترودهای غلتکی گوی دار و استوانه ای و برداشتن اندومتر توسط الکترود حلقه ای بکار رفتند. نشان داده شده که استفاده قبل از عمل آگونیست های GnRH میزان موفقیت را پس از برداشتن یا Ablation آندومترافزایش می دهد.Donnez و همکارانش در یک مطالعه وسیع چند مرکزی که بصورت تصادفی و دو سوکور و کنترل شده با دارونما (Placebo controlled) انجام شده است در مقایسه بین آگونیست های GnRH،و دارونما قبل از Ablation آندومتر،افزایش می دهد. Donnez و همکارانش در یک مطالعه وسیع چند مرکزی که بصورت تصادفی و دو سوکور و کنترل شده با دارونما (Placebo controlled) انجام شده است در مقایسه بین اگونیست های GnRH، 40% و در مقابل نزد استفاده کنندگان ازآگونیست های GnRH و دارونما قبل از Ablation آندومتر،نشان دادند که میزان آمنوره در دو سال نزد استفاده کنندگان از دارونما 26% بوده است.درمجموع میزان آمنوره پس از Ablation آندومتر،بین 25 تا 60 درصد با تمایل به سوی میزان بالاتر نزد کسانی که با فواصل کوتاهتری پیگیری شده اند، است.بنظر می رسد در کوتاه مدت جهت منوراژی Ablation آندومتر بر هیسترکتومی مزیت اقتصادی داشته باشد. با این حال،دریک مطالعه 34% زنانی که Ablation آندومتر شده بودند طی 5 سال هیسترکتومی شدند.رضایت از این عمل در بیشتر مطالعات به 90% می رسد.
برداشتن (رزکسیون) آندومتر با استفاده از یک الکترود حلقه ای وبا جریانی برشی با 100 وات انرژی بصورت
نوارهای 4 میلی متری مجاورهم انجام می شود که از قدام شروع شده و تا 360درجه پیش می رود.
اگر Ablation آندومتر توسط غلتک گوی دار انجام می شود باید مراقب بود تا از Ablation بافت آندوسرویکس به منظور جلوگیری از بروزتنگی گردن رحم بصورت Iatrogenic،پرهیز شود.برای این کار می توان ابتدا یک حلقه 360 درجه ای را دور تا دور مرز بین آندوسرویکس و حفره داخل رحمی،کوتریزه کرده تا محدوده Ablation مشخص شود.ابتدا باید فوندوس و جداره قدامی را Ablation شاخ رحم در انتها صورت گیرد زیرا این ناحیه بیشترین احتمال سوراخ شدن را دارد و می تواند منجر به توقف عمل شود.برای جلوگیری از سوراخ شدن،غلتک گوی دار را باید به ملایمت برروی ناحیه شاخ رحم فشار داد. عوارض در تقریباً 12% موارد ایجاد شده شامل سندرم اضافه بار مایع و سوراخ شدن رحم می باشند.بندرت یک کانسرآندومتر یا حاملگی تشخیص داده نشده و موجب بروز مشکل در این عمل می شود
منبع:مامایی و بیماریهای زنان دنفورث (جلد دوم).
/ج