کارسینوم مهاجم سرویکس
خصوصیات بالینی
شکایات تظاهرکننده
شایع ترین شکایت کانسر سرویکس خونریزی یا ترشح غیر طبیعی واژینال است. خونریزی غیر طبیعی ممکن است به شکل لکه بینی بعد از مقاربت، خونریزی بین قاعدگیها، منوراژی، یا لکه بینی پس از یائسگی باشد. اگر خونریزی مزمن باشد، بیمار ممکن است از خستگی یا سایر شکایات مربوط به آنمی شکایت کند. ترشح واژینال خونابه ای یا زرد،غالباً همراه با بوی زننده ممکن است با کارسینوم پیشرفته یا نکروتیک همراه باشد. درد لگنی ممکن است از بیماری پیشرفته موضعی یا نکروز تومور ناشی شود. گسترش تومور به دیواره جانبی لگن ممکن است منجر به درد سیاتیک یا درد پشت همراه با هیدرونفروز شود. تومور متاستاتیک به عقده های لنفاوی ایلیاک و پاراآئورتیک می تواند بداخل ریشه های اعصاب لومبوساکرال گسترش یابد و بصورت درد پشت لومبوساکرال تظاهرکند. شکایات ادراری یا رکتال (هماچوری، هماتوشزی) می توانند با تهاجم به مثانه یا رکتوم توسط کارسینوم سرویکس با درجه پیشرفته همراه باشند.
یافته های فیزیکی
کارسینوم مهاجم سرویکس طیف وسیعی از نماهای بالینی را نشان می دهد. ضایعات زودرس ممکن است بطور موضعی قرمز شده یا زخمی باشند و یا بصورت نواحی مختصراً برجسته و گرانولری تظاهر کنند که به آسانی در اثر تماس خونریزی کنند (شکال15). تومورهای پیشرفته تر دو نوع نمای بالینی اصلی دارند: اگزوفیتیک و آندوفیتیک. تومورهای اگزوفیتیک مشخصاً نمای پولیپوئید یا پاپیلر دارند. تومورهای آندوفیتیک عموماً اولسره یا ندولر می باشند. آنها تمایل دارند که در داخل کانال آندوسرویکال بروز کنند و غالباً بطور عمیق بداخل استرومای سرویکس تهاجم می کنند و یک سرویکس بزرگ شده سفت بشکه ای شکل بوجود می آورند.
گسترش بیماری
گسترش پاراسرویکال و پارامتریال
سلولهای تومور بطور شایعی از طریق عروق لنفاوی پارامتریال پخش می شوند و به عقده های لنفی پارامتریال گسترش می یابند و درآنها جایگزین می شوند (شکل 16).این توده های توموری منفرد بزرگ می شوند وبا هم تلاقی می کنند و نهایتاً جایگزین بافت طبیعی پارامتریال می شوند. با شیوع کمتری، توده مرکزی تومور با گسترش پیوسته مستقیم از طریق لیگامان کاردینال (Mackenrodt's) به دیواره جانبی لگن می رسد. درگیری بارز بخش مدیال این لیگامان ممکن است منجر به انسداد حالب شود.
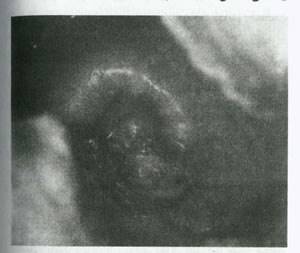
شکل 15.نمای بالینی کارسینوم سلول سنگفرشی سرویکس این ضایعه از نوع اولسراتیو است.
گسترش واژینال
هنگامی که تومور اولیه به ورای مرزهای سرویکس گسترش یافته است، قسمت فوقانی واژن اغلب درگیر می شود (0/050موارد). گسترش قدامی از طریق سپتوم وزیکوواژینال از همه شایعتر است که اغلب سطح فاصل بین مثانه و تومور سرویکس زیرین را محو می کند و درمان جراحی را مشکل یا غیر ممکن می سازد. از سمت خلف یک کولدوساک (بن بست دوگلاس) پریتونئومی عمقی می تواند بعنوان سد آناتومیکی عمل کند که گسترش تومور را از سرویکس و واژن به سمت رکتوم هدایت کند.
درگیری مثانه و رکتوم
گسترش قدامی و خلفی کانسر سرویکس به مثانه و رکتوم در غیاب بیماری پارامتریال لترال شایع نیست. تنها در 0/020بیماران با گسترش توموربه دیواره جانبی لگن،تهاجم به مثانه در بیوپسی قابل اثبات است.
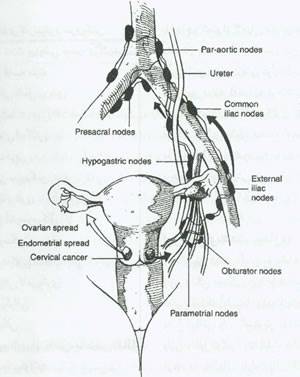
شکل 16.مسیرهای آناتومیک گسترش در کارسینوم مهاجم سرویکس.
درگیری اندومتر
آندومتر در 0/02 تا 0/010 موارد کانسر سرویکس درمان شده با جراحی درگیر شده است، اگر چه شیوع کلی (شامل موارد غیر جراحی) نامعلوم است. گسترش به آندومتر با کاهش شانس بقاء و شیوع بیشتر متاستازهای دوردست همراه است.
متاستاز تخمدانی
درگیری تخمدان با کانسرسرویکس نادر است، ولی در صورت وجود،به احتمال بیشتر ازطریق ارتباطات لنفاوی بین رحم و ساختمانهای ضمائم رحم اتفاق می افتد. در بیمارانی که تحت درمان جراحی قرار می گیرند،متاستازهای تخمدانی در کمتر از 1% کارسینومهای سلول سنگفرشی و مختصری بیش از 0/01آدنوکارسینومها وجود دارند.
درگیری عقده های لنفاوی
گسترش لنفاوی کارسینوم سرویکس طرح منظم و منطقی قابل پیش بینی را دنبال می کند.دسته های عقده های لنفاوی که با شیوع درگیر می شوند،عبارتند از ابتوراتور،ایلیاک خارجی و هیپوگاستریک. عقده های لنفی گلوتئال تحتانی و پره ساکرال با شیوع کمتری درگیر می شوند. درگیری عقده ای ثانویه (یعنی ایلیاک مشترک و پاراآئورتیک) ندرتاً در غیاب بیماری عقده ای اولیه (یعنی لگنی) اتفاق می افتد. درصد درگیری عقده های لنفاوی مستقیماً با حجم تومور اولیه افزایش می یابد. ندرتاً،آمبولیزه شدن لنفاوی پس گرا ممکن است به عقده های لنفاوی اینگوینال اتفاق افتد. دربیماران با بیماری پیشرفته یا عود کننده ممکن است گسترش با متاستاز در عقده های اسکالن یافت شود.
گسترش خونی
شایعترین نواحی برای گسترش خونی ریه، کبد و استخوان می باشد. متاستاز به روده ،غده فوق کلیوی، طحال و مغز شیوع کمتری دارند.
تشخیص و درجه بندی
یک قرارداد بین المللی برای درجه بندی مقایسه نتایج بین موسسات مختلف و تعاریف کدهای درمانی در درون یک
جدول5:روشهای درجه بندی کارسینوم سرویکس
|
معاینه ی بالینی /معاینه تحت بیهوشی توصیه می شود .
مطالعات رادیولوژی عکس داخل وریدی
پیلوگرافی داخل وریدی
باریوم انما
عکسهای اسکلتی
روش ها/کولپوسکوپی
بیوپسی سرویکس
مخروط برداری
کورتاژ آندوسرویکال
سیستوسکوپی
پروکتوسکوپی
مطالعات اختیاری/توموگرافی کامپیوتری
لنفانژیوگرافی
سونوگرافی
تصویر برداری با رزونانس مغناطیسی (mri)
اسکن رادیونوکلئید
لاپاروسکوپی/لاپاروتومی
|
موسسه را امکانپذیر می سازد. فدراسیون بین المللی زنان و زایمان (FIGO) سیستم درجه بندی برای تشخیص و ارزیابی کارسینوم سرویکس دارد که بر پایه ارزیابی های بالینی (مشاهده ،لمس،کولپوسکوپی)، آزمایشات رادیوگرافیک قفسه سینه، کلیه ها و اسکلت، و ECC و بیوپسی ها می باشد. لنفانژیوگرافی،ارتریوگرافی،اسکن های توموگرافی کامپیوتری (CT)،تصویر برداری با رزونانس مغناطیسی (MRI) و لاپاروسکوپی یا لاپاروتومی نباید برای درجه بندی بالینی مورد استفاده قرار گیرند. روشهای درجه بندی مجاز به واسطه قرار داد FIGO در جدول 5 نشان داده شده است.
FIGO در سال 1995 سیستم درجه بندی بالینی کارسینوم سرویکس را مورد بازنگری قرار داد (جدول6) نئوپلاسم های درجه I آنهایی هستند که از لحاظ بالینی به سرویکس محدود می باشند. در طبقه بندی جاری درجه IA1 (کارسینوم با تهاجم میکروسکوپی) بصورت توموری تعریف می شود که تهاجم به استروما درآن به عمق بیش از 3 میلی متر غشای پایه نبوده و عریض تر از 7 میلی متر نباشد. این تعریف منعکس کننده اطلاعاتی است دال براینکه بیماران با تهاجم کمتر از 3 میلی متر در معرض خطر بسیار کمی برای متاستاز بیماری قرار دارند و می توان آنها را بطور محافظه کارانه تری مورد درمان قرار داد. سیستم درجه بندی 1995 همچنین درجه IB را به درجات فرعی IB1 (باقطرحداکثر چهار سانتی متر یا کمتر) و IB2(بزرگتر از4cmدر قطر حداکثر) تقسیم می کند که این نشان دهنده اهمیت حجم تومور در ضایعات ماکروسکوپی محدود به سرویکس است. توزیع بیماران بر حسب درجه بالینی بدین قرار است :درجه I38%، درجه II 32%، درجه III 26% و درجه IV 4%.
ارزیابی وسعت بیماری
تعیین درجه بالینی به مشاهده و لمس دقیق سرویکس، واژن ولگن بستگی دارد. باید تمام واژن را لمس کرد تا بتوان تعیین کرد که آیا بیماری محدود به سرویکس می باشد (IB)، به 2/3 فوقانی واژن گسترش یافته است (IIA)، یا 1/3 تحتانی واژن را نیز درگیر کرده است(IIIA) (شکل 17)، گسترش تومور به بافتهای پارامتریال (IIB) یا به دیواره جانبی لگن (IIIB) با معاینه رکتوواژینال بهتر از همه قابل کشف است. با معاینه بالینی تعیین اینکه آیا یک پارامتریوم صاف ولی قرمز شده، واقعاً مبتلا به کانسر است یا تنها ملتهب شده است غیر ممکن است و بیمار باید تنها درصورتی به عنوان درجه III تشخیص داده شود که پارامتریوم در دیواره لگنی ندولر باشد یا رشد بیماری به دیواره لگن گسترش یافته باشد.
هنگامی که شکی در رابطه با درجه یک تومور وجود داشته باشد، انتخاب درجه پایین تر ضرورت دارند. هنگامی که درجه بالینی تعیین درمان آغاز شد، یافته های بعدی در ادامه درجه بندی بالینی (CT و غیره) یا اکتشاف جراحی نباید درجه تخصیص داده شده را تغییردهند. اختصاص دادن یک درجه پیشرفته تر در طی درمان منجر به بهبود آشکار ولی فریبنده نتایج درمان جهت بیماری با درجه پایین تر می باشد.
درجه بندی جراحی
طبقه بندی جاری درجات FIGO برای کانسر سرویکس بر پایه یافته های بالینی قبل از درمان است. تنها زیرگروههای فرعی درجه IA1, IA2) I) نیاز به ارزیابی پاتولوژیک دارند. تفاوتهای بین درجه بندی بالینی و یافته های جراحی و پاتولوژی در دامنه 17/3% تا 38/5% در بیماران با درجه بالینی I و 42/9% تا 89/5% در بیماران
جدول 6.درجه بندی flogبرای کارسینوم سرویکس
|
در جه
|
خصوصیات
|
|
O
|
کارسینوم درجا،کارسینوم داخل اپیتلومی
|
|
I
|
کارسینوم تنها معدود به سرویکس می باشد
|
|
IA
|
کانسر مهاجم تنها بصورت میکروسکوپی کشف می شود.تمام ضایعات قابل رویت حتی با تهاجم سطحی در درجه IB قرار می گیرند.تهاجم اندازه گیری شده استروما به ?5 میلی متر عمق و <7 میلی متر عرض
|
|
IA1
|
تهاجم اندازه گیری شده استروما ≤3میلی متر در عمق و <7 میلی متر در عرض
|
|
IA2
|
تهاجم اندازه گیری شده استروما>3میلی متر ولی ≤5میلی متر در عمق< 7 میلی متر در عرض
|
|
IB
|
ضایعات بالینی محدود به سرویکس یا ضایعات قبل از مرحله بالینی بزرگتر از درجه
|
|
IB1
|
ضایعات بالینی به اندازه ≤4 سانتی متر
|
|
IB1
|
ضایعات بالینی به اندازه >4 سانتی متر
|
|
II
|
کارسینوم به ورای سرویکس گسترش یافته است ولی به دیواره لگن نرسیده است.کارسینوم واژن را درگیر کرده است ولی به 1/3 تحتانی نمی رسد
|
|
IIA
|
درگیری واضح پارامتریال وجود ندارد .
|
|
IIB
|
درگیری واضح پارامتریال
|
|
III
|
کارسینوم به دیواره لگن گسترش یافته است.در معاینه رکتوم فضای فاقد کانسر بین تومور و دیواره لگن وجود ندارد.تومور 1/3 تحتانی واژن را درگیر کرده است.تمام موارد هیدرونفروز یا کلیه های بدون عملکرد در این درجه جای می گیرد،مگر اینکه به علت دیگری شناخته شده باشد
|
|
IIIA
|
گسترش به دیواره لگن وجود ندارد .
|
|
IIIB
|
گسترش به دیواره لگن،هیدرونفروز ،یا کلیه فاقد عملکرد
|
|
IV
|
کارسینوم به ورای لگن حقی گسترش یافته یا از لحاظ بالینی مخاط مثانه یا رکتوم را درگیر کرده است.ادم بولوز اجازه اختصای دادن یک بیمار به درجه IVرا می دهد .
|
|
IVA
|
گسترش رشد به ارگانهای مجاور
|
|
IVB
|
گسترش به ارگانهای دوردست.
|
قرار می گیرند. این امر منجر شده است تا بعضی بر درجه بندی جراحی کارسینوم سرویکس برای شناسایی گسترش مخفی تومور و تعیین وجود بیماری خارجی لگنی تایید نمایند، به نحوی که درمانهای اضافی یا گسترش دادن دامنه اشعه تابی قابل پیشنهاد باشند. روشهای درجه بندی جراحی ترانس پریتونئال اگربا اشعه تابی شکم و لگن دنبال شوند،خصوصاً در مورد حرکات روده ها با عوارض محسوسی همراه خواهند بود. دسترسی جراحی اکسترا پریتونئال از طریق یک برش پاراامبلیکال یا پارامدین قابل انجام می باشد و ارزیابی دقیق وضعیت بیماری را امکان پذیر می سازد.این روش با عوارض کمی همراه بوده،شروع درمان اشعه تابی را به تأخیر نمی اندازد. نقش درجه بندی جراحی لاپاروسکوپی برای کانسر سرویکس هنوز تعیین نشده است.
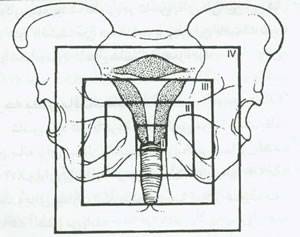
شکل 17.درجات بالینی کارسینوم سرویکس .در درجه Iتنها سرویکس درگیر است در درجه IIپارامتریوم یا 2/3 فوقانی واژن درگیر است.در درجه IIIبدخیمی به دیواره جانبی لگن گسترش یافته یا 1/3 تحتانی واژن را درگیر می کند.
متغیرهای با اهمیت درپیش آگهی
خصوصیات تومور
متغیرهای با اهیمت در پیش آگهی،مستقیماً با خصوصیات جراحی و پاتولوژی تومور مرتبط بوده و تاثیر آنها بر شانس بقای بیماران به وسیله برنامه های نقشه برداری، اپیدمیولوژی و نتایج نهایی (NCI (SEER برای دوران 1973 تا 1987 جمع آوری شدند. این مطالعه شامل 17119 بیمار با کانسر مهاجم سرویکس بود و به این نتیجه رسیدکه در FIGO،بافت شناسی تومور، درجه بافت شناسی و وضعیت عقده های لنفاوی همگی متغیرهای پیش آگهی مستقلی می باشند که با شانس بقا مرتبط اند. بعلاوه حجم تومورو عمق تهاجم نیز بر شانس بقا موثر نشان داده شده اند.
درجه
درجه بالینی بیماری در زمان بروز، مهمترین تعیین کننده شانس بقاء صرفنظر از روش درمان،است.شانس بقاء پنج ساله به موازاتی که درجه FIGO در هنگام تشخیص از درجه IA به درجه IV افزایش می یابد،از 97% به 12/4% کاهش می یابد. شانس بقا برای هر درجه ای در مقایسه با درجه IA بوضوح کمتر است.
بافت شناسی
کارسینوم های سنگفرشی مسئول 74/9% بیماران در داده های SEER می باشند، درحالی که 15/1% از موارد، آدنوکارسینوم بودند. تفاوتی در شانس بقای کلی بین این دو زیر گروه بافت شناسی دیده نشد.با وجود این بافت شناسی آدنواسکوآموس با کاهش شانس بقا همراه بود.
درجه بندی بافت شناسی
شانس بقاء کلی با درجه تمایز تومور مرتبط است. بقاء پنج ساله برای بیماران با تومورهای بخوبی تمایز یافته 74/5% و برای بیماران با تومورهای با تمایز متوسط 63/7% است و برای بیماران با کارسینومهای با تمایز ضعیف به 51/4% کاهش می یابد.
درگیری عقده های لنفاوی
در میان بیماران تحت درمان جراحی قرار گرفته،شانس بقاء مستقیماً با تعداد و محل قرار گیری متاستازی های عقده های لنفاوی در ارتباط است. شیوع عقده های لنفاوی مثبت با درجه بیماری افزایش می یابد (جدول 7). هنگامی که عقده های لنفاوی لگنی و پاراآئورتیک هر دو منفی باشند، میزان بقاء پنج ساله برای تمام درجات بیماری 75/2% است. شانس بقاء با عقده های لگنی مثبت به 45/6% کاهش می یابد و خطر عود با تعداد عقده های درگیر مرتبط است. میزان عود با یک عقده لنفاوی لگنی مثبت 35%، با دو یا سه عقده لگنی مثبت 0/059، وبا متاستاز به بیش از سه عقده لنفاوی لگنی 0/069 است هنگامی که عقده های پاراآئورتیک درگیرباشند، میزان بقاء پنج ساله به 15/4% کاهش می یابد.
حجم تومور
سیستم درجه بندی بازبینی شده FIGO برای کانسر سرویکس منعکس کننده این حقیقت است که اندازه ضایعه عامل پیشگویی کننده مهمی برای شانس بقاء است. با وجود این ، Finan و همکاران (1996) نشان دادند که تقسیم بیماران درجه IB به زیرگروههای IB1 و IB2 ضرورتاً تاثیر مستقلی بر شانس بقاء ندارد. بلکه در بیماران درجه IB1 ترجیحاً اندازه ضایعه از طریق وضعیت عقده ها تاثیر خود را بر شانس بقاء محقق می سازد. حجم بزرگتر تومور با میزان بیشتر درگیری پارامتریال و کاهش شانس بقاء همراه است. برای درجات از IB به IIB میزان بقاء پنج ساله هنگامی که پارامتر با تومور درگیر باشد از 84/9% به 69/6% کاهش می یابد.
عمق تهاجم
شانس بقاء قویاً با عمق تهاجم تومور بداخل استروما مرتبط است و میزان بقاء سه ساله برای تهاجم کمتر از 10 میلی متر 86% تا 94%، برای تهاجم 11 تا 20 میلی متر 71% تا 75% و برای تهاجم بیش از 21 میلی متر 60% است.
عوامل میزبان
سن
اینکه زنان جوانتر در مقایسه بازنان مسن تر با درجه بیماری یکسان میزان بقاء کمتری دارند یا خیر هنوز مورد اختلاف نظر است. بعضی محققین کاهش شانس بقاء را در زنان جوانتر از 35 تا 40 سال مشاهده کرده اند، البته این بیماران شیوع بیشتری از تومورهای با تمایز ضعیف دارند. سایرین تفاوت بارزی در شانس بقاء بین بیماران جوانتر و
مسن تر نیافته اند.
عوامل خونی
شیوع آنمی قبل از درمان (هموگلوبین 12 گرم در دسی لیتر یا کمتر)با پیشرفت درجه بیماری افزایش می یابد و به ترتیب 25%، 33% و 45% بیماران با بیماری درجه II,I و IV اتفاق می افتد.آنمی با شیوع بیشتر عودهای لگنی و کاهش شانس بقاء همراه است که عمدتاً بعلت شیوع بیشتر شکست اشعه درمانی است.هیپوکسی تومور مکانیسم پیشنهادی مقاومت به اشعه در حضور آنمی است.یک پارامتر خونی پیش آگهی دهنده دیگر ترومبوسیتوز (بیش از 400000 در میلی متر مکعب) است که پس از کنترل از لحاظ نوع سلول،درجه و سن با کاهش شانس بقاء همراه بوده است.
وضعیتهای بیماری همراه
دیابت و فشارخون غالباً با بیماری عروقی بارز همراهند و بالقوه هم در هیپوکسی تومور و هم در کاهش خونرسانی به بافتهای طبیعی لگن سهیم می باشند. بیماران مبتلا به این بیماریها در معرض شیوع بیشتر عوارض درمان و عود تومور لگنی و کاهش شانس بقاء قرار دارند.
آسیب شناسی
کارسینوم سلول سنگفرشی (SCC) 0/075تا 0/090 موارد کانسر سرویکس را تشکیل می دهد و می توان آنرا بطور قراردادی به سه درجه بافت شناسی مختلف تقسیم کرد.
جدول 7.شیوع متاستازهای عقده های لنفاوی لگنی وپارااآئورتیک بواسطه ی درجه flog کارسینوم سرویکس
|
عقده های پاراآئورتیک مثبت (0/0)
|
عقده های لگنی مثبت
(0/0)
|
n
|
درجه
|
|
0
|
5/0
|
179
|
IA
|
|
1>
|
2/6
|
178
|
IA2
|
|
2/2
|
9/15
|
1926
|
IB
|
|
11
|
5/24
|
110
|
IIA
|
|
19
|
4/31
|
324
|
IIB
|
|
30
|
8/44
|
125
|
III
|
|
40
|
55
|
23
|
IVA
|
SCC درجه یک
درجه یک (Grade 1) تومور بخوبی تمایز یافته ای است که از صفحات و طنابهای سلولی با سیتوپلاسم اسید وفیلیک فراوانی تشکیل شده است که پلهای بین سلولی بوضوح قابل رویتی دارند و اغلب مقادیر متغیری کراتین تولید می کنند. تشکیل یک مروارید اپیدرموئید مشخصه این تومورهای بخوبی تمایزیافته است که میتوزها نسبتاً کمی درآنها یافت می شوند. تومورهای درجه یک حدود scc5% های سرویکس را تشکیل می دهند.
SCC درجه دو
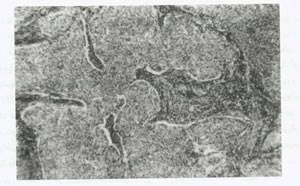
درجه دو (Grade 2) شایعترین نوع بوده SCC 85% ها در این دسته قرار می گیرند (شکل18).این تومور با توده ها و طنابهای سلولهای سنگفرشی دوکی شکل با هسته های طویل و سیتوپلاسم کم مشخص می شود ممکن است نواحی معدودی وجود داشته باشند که سلولهای بزرگ شده و بخوبی تمایز یافته باشند تا مرواریدهایی را تشکیل دهند،ولی در کل پلهای بین سلولی وجود ندارند و میزان تشکیل کراتین کم است.تعداد میتوزها بیش از تومورهای بخوبی تمایزیافته است.
SCC درجه سه
تومورهای درجه سه (Grade 3) یا تمایز نیافته،میزان رشد سریعی دارند و میتوزهای بسیار زیاد و سلولهای با هسته هایی بغایت شلوغ و سیتوپلاسم اندک در آنها دیده می شود. این تومورها را به سختی می توان منشاء گرفته از سلولهای سنگفرشی دانست. این موارد تقریباً 0/010 SCCهای سرویکس را تشکیل می دهند.
درمان
اداره عمومی بیماران بواسطه درجه تومور
جراحی و اشعه تابی دو روش درمان می باشند که بیش از همه برای درمان کارسینوم مهاجم سرویکس بکار گرفته می شوند.بطورکلی، درمان اولیه جراحی به درجات I و IIA محدود می شود. مزایای زیاید برای درمان جراحی نسبت به اشعه تابی وجود دارند. جراحی امکان اکتشاف کامل لگن و شکم را فراهم می سازد که می توان بیماران با اختلاف بین
درجات بالینی و جراحی - آسیب شناسی را بدین وسیله شناسایی کرد. چنین بیمارانی را می توان سپس تحت طرح درمانی انفرادی براساس وضعیت دقیق بیماری شان قرار داد. در بیماران جوانتر، جراحی امکان حفظ تخمدانها را فراهم می کند که می توان تخمدانها را به خارج از موضع اشعه تابی بعدی جابجا کرد. هیسترکتومی رادیکال منجر به کوتاه شدن واژن می شود، با وجود این، با فعالیت جنسی طویل شدن تدریجی اتفاق خواهد افتاد.
تشکیل فیستول مجاری ادراری و روده ها و عوارض محل برش درمان جراحی ترجیحاً در زمان زودرس تری در دوران بعد از عمل اتفاق می افتند و معمولاً قابل اصلاح با ترمیم جراحی هستند. سایر دلایل انتخاب درمان جراحی رادیکال نسبت به اشعه تابی مشتملند بر بیماری التهابی همزمان روده، اشعه تابی قبلی جهت بیماریهای دیگر، و وجود نئوپلاسم همزمان ضمائم رحم.
اشعه درمانی را می توان برای تمام درجات بیماری و برای بیشتر بیماران صرفنظر از سن، وضعیت بدنی، یا بیماریهای همزمان مورد استفاده قرار داد.عملکرد جنسی ممکن است به مخاطره بیفتد، چرا که اشعه تابی به لگن، فیبروز پایدار و واژن و آتروفی آنرا همراه با کاهش قطر وطول واژن ایجاد می کند. عملکرد تخمدان تقریباً در تمام بیمارانی که تحت اشعه درمانی به لگن قرار می گیرند از دست می رود. برخلاف درمان جراحی، عوارض فیستولی مرتبط با درمان اشعه تابی در زمان دیرتری اتفاق می افتند و ثانویه به عروقی شدن ضعیف بافتها به علت فیبروز و واسکولیت وابسته به اشعه ترمیم مشکلتری دارند.
درجه IA1
میزان بقاء پنج ساله این بیماران با درمان اولیه جراحی تقریباً به صد درصد می رسد. هیسترکتومی اکسترافاشیال برای این گروه از بیماران درمان کافی است. اگر حفظ باروری مورد نظر باشد مخروط برداری را می توان بطور انتخابی مورد استفاده قرار داد مشروط براینکه حاشیه های جراحی عاری از بیماری باشد. در غیاب تهاجم لنفی عروقی،شیوع متاستازهای عقده های لنفاوی لگنی 0/3% است و اندیکاسیونی برای لنفادنکتومی وجود ندارد.با وجود درگیری لنفی - عروقی، خطر متاستازهای عقده های لگنی به 2/6% داخل حفره ای مورد درمان قرار داد.
درجه IA2
کارسینوم با تهاجم میکروسکوپی و تهاجم به استروما 3/1 تا 5 میلی متر با عقده های لنفی لگنی مثبت در 62 درصد بیماران همراه است. درمان ارجح برای این ضایعات هیسترکتومی رادیکال تعدیل شده (نوع II) همراه با لنفادنکتومی لگنی است.
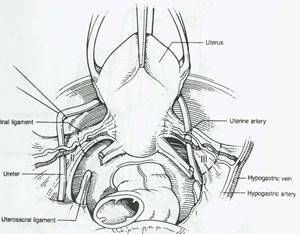
شکل 19.تشریح آناتومیک هیسترکتومی رادیکال لیگامانهای کاردینال در سطح حالب (نوع II)یا در سطح دیواره ی جانبی لگنی (نوع III)قطع شده اند(خطوط نقطه چین)
درجات IIA, IB2, IB1
درمان جراحی و اشعه تابی هردو به یک اندازه در درمان کارسینوم درجات IB و IIA سرویکس موثرند.مطالعات کنترل نشده بی شماری از مزایای هر یک ازاین روشهای درمانی حمایت می کنند و تفاوت بارزی در کنترل تومور لگنی یا شانس بقاء کلی بین آنها وجود ندارد. Zander و همکاران 1092 بیمار را با کانسر سرویکس درجات IB و II گزارش کردند که تحت درمان هیسترکتومی رادیکال (نوع III) و لنفادنکتومی لگنی قرار گرفتند.میزان بقاء پنج ساله برای درجه 84/5 IB% و برای درجه II 71/1% بود. با درمان اشعه تابی اولیه میزان بقاء مشابهی بدست می آید. Perez و همکاران (1986) در یک مطالعه سری میزان بقاء 5 ساله 85% را برای 312 بیمار با بیماری درجه IB و 70% برای 98 بیمار با بیماری درجه IIA گزارش کردند که تحت درمان اولیه اشعه تابی قرار گرفتند.
برای بیماران با تومورهای درجه یک حجیم (IB2) درمان باید بطور فردی انتخاب شود. گسترش تومور به آندوسرویکس فوقانی و قطعه تحتانی رحم آناتومی طبیعی سرویکس را بهم می ریزد و منجر به قرارگیری منشاء اشعه تابی داخل حفره ای در محلی غیرایده آل می شود. نتیجتاً، میزان شکستگی تا حد 17/5% در بیماران با ضایعات سرویکس بزرگتر از شش سانتی متر که تحت درمان با اشعه تابی تنها قرار گرفته اند گزارش شده است. در چنین شرایطی هیسترکتومی اکسترافاشیال تکمیلی معمولاً بدنبال درمان اشعه تابی انجام می شود.
اگرچه بسیاری از پزشکان استفاده از درمان هیسترکتومی رادیکال را به بیماران با ضایعات کوچک درجه IB( کمتر3 تا 4 سانتی متر) یا درجه IIA محدود می دانند، شواهدی وجود دارند که میزان بقاء قبولی با درمان اولیه جراحی در بیماران با بیماری حجیم محدود به سرویکس قابل حصول می باشد.میزان بقاء 5 ساله برای ضایعات سرویکس بزرگتر از 4 سانتیمتر پس از هیسترکتومی رادیکال ولنفادنکتومی لگنی در دامنه 73/6% تا 82% قرار دارد. برای ضایعات بزرگتر از 6 سانتی متر شانس بقاء 5 ساله به 66% کاهش می یابد.
درجات IVA, III, IIB و IVB
برای بیماران با بیماری درجه IIB ودرجات بالاتر،
درمان اشعه تابی درمان انتخابی است. درمان اشعه تابی برای کانسر مهاجم سرویکس بصورت ترکیبی از درمانهای خارجی و داخل حفره ای بکارگرفته می شود. میزان بقاء طویل المدت برای درجه II تقریباً 60%، برای درجه III 35% و برای درجه IV 18% است. بیماران با بیماری درجه IVB معمولاً با شیمی درمانی تنها یا شیمی درمانی همراه با اشعه تابی موضعی درمان می شوند. صرفنظر از روش درمان، تابی موضعی درمان می شوند. صرفنظر از روش درمان، این بیماران همه پیش آگهی ضعیفی دارند.
درمان جراحی
انواع هیسترکتومی
5 نوع مجزا از هیسترکتومی در درمان کانسر سرویکس مورداستفاده قرار می گیرد.
نوع I:هیسترکتومی نوع I به هیسترکتومی شکمی کامل اکسترافاشیال اطلاق می شود. این روش برداشتن کامل سرویکس را همراه با حداقل از هم گسیختگی ساختمانهای اطراف تضمین می کند و درمان مناسبی برای بیماری درجه IA1 است.
نوع II: هیسترکتومی نوع II به عنوان هیسترکتومی رادیکال تعدیل شده یا هیسترکتومی Wertheim اطلاق می شود(اشکال 19 تا 21). این روش جداکردن حالبها از بافتهای پارامتریال و پاراسرویکال را تا محل تلاقی حالب و مثانه به همراه دارد. این امر برداشتن تمام بافت پارامتریال داخل حالبها و همچنین نیمه مدیال لیگامان یوتروساکرال و 1 تا 2 سانتی متر پروگزیمال واژن را امکان پذیر می سازد. این جراحی را می توان همراه با لنفادنکتومی لگنی انجام داد.
نوع III: در هیسترکتومی شکمی رادیکال (Meigs) یا نوع III حالبها بطور کامل از کانال پاراسرویکال جدا می شوند و مثانه ورکتوم وسیعاً برای حرکت دادن آزاد می شوند (اشکال19 تا 21). برقرار ساختن فضاهای پاراوزیکال و پارارکتال برداشتن تمام بافت پارامتریال را تا دیواره جانبی لگن، برداشتن کامل لیگامانهای یوتروساکرال،و برداشتن 1/3 تا نیمه فوقانی واژن را تسهیل می کند. لنفادنکتومی لگنی دو طرفه همراه با این عمل انجام می شود.
نوع IV/نوع V: هیسترکتومی رادیکال گسترش یافته یا نوع IV برداشتن شریان وزیکال فوقانی، بافت اطراف رحم، و تا 3/4 فوقانی واژن را شامل می شود. در جراحی نوع V یا جراحی در آوردن نسبی احشاء حالبهای دیستال و بخشی از مثانه خارج می شوند. اعمال جراحی نوع IV و نوع V یا امروزه به ندرت انجام می شوند چرا که بیشتر بیماران با بیماری گسترده به حدی که نیاز به این اعمال جراحی داشته باشند را می توان با کفایت بیشتری بوسیله درمان اولیه اشعه درمانی مورد درمان قرار داد.
عوارض هیسترکتومی شکمی رادیکال
بیهوشی و تکنیکهای جراحی مدرن،مرگ و میر جراحی هیسترکتومی رادیکال را به 0/6% کاهش داده اند. آمبولی ریوی بالقوه کشنده در 1 تا 2% ازبیماران اتفاق می افتد. فیستولهای یورتروواژینال و وزیکوواژینال به ترتیب در 2% و 0/9% اتفاق می افتد. شایعترین عارضه مشاهده شده به دنبال هیسترکتومی رادیکال اختلال عملکرد ادراری است که از دنرواسیون نسبی عضله دترسور در حین برش بافتهای پاراسرویکال و پاراواژینال ناشی می شود. تشکیل کیست لنفی لگنی در 2% تا 6/5% بیماران متعاقب هیسترکتومی رادیکال و لنفادنکتومی لگنی بوقوع می پیوندد. شیوع آن هنگامی که فضاهای رتروپریتونئال باز گذاشته شوند کمتر می شود. اغلب کیست های لنفی بدون علامت هستند و نیاز به مداخله درمانی ندارند با وجود این گاهی ممکن است کیستهای لنفی موجب درد لگنی، انسداد حالب، یا انسداد وریدی نسبی همراه با ترومبوز شود.
درمان اضافی متعاقب جراحی
اطلاعات محدودی در خصوص موثر بودن اشعه درمانی لگنی پس از عمل جراحی در بیماران در معرض خطر بالای عود پس از هیسترکتومی رادیکال و لنفادنکتومی لگنی وجود دارد. عوامل خطرزای پیش آگهی مشتملند بر تهاجم میکروسکوپی به پارامتر، متاستازهای عقده های لنفاوی لگنی، تهاجم عمقی سرویکال،و حاشیه های جراحی مثبت
یا بسته. بهبود شانس بقاء بدنبال درمان اشعه تابی پس از جراحی برای بیماران با یک یا دو عقده لگنی مثبت هنوز به خوبی نشان داده نشده است. اگر چه مطالعات کنترل شده ای وجود ندارد، اطلاعات گذشته نگر پیشنهاد کننده این مطلب هستند که اشعه تابی پس از جراحی بدنبال هیسترکتومی رادیکال ممکن است افزایش متوسطی را در شانس بقاء بیماران با سه یا چهار عقده لنفی لگنی مثبت ایجاد کند. با این حال، درمان جراحی و اشعه درمانی توام منجر به افزایش ناتوانی می شود، همچنانکه لنفادم اندام تحتانی در 23/4% از بیمارانی که درمان توام دریافت می کنند گزارش شده است.
تجویز عوامل شیمی درمانی قبل از رادیکال هیسترکتومی را به عنوان شیمی درمانی اضافی جدید نامیده اند. سپس پلاتین (Platinol)، سولفات بلئومایسین (Blenoxane)، وسولفات ون بلاستین (Velban) گسترده تر از سایر ترکیبات مورد استفاده قرار گرفته اند. هنگامی که ازسایرترکیبات مورد استفاده قرارگرفته اند. شیمی درمانی قبل از جراحی تجویز می شود میزان پاسخ بالینی کامل دردامنه 17% تا 43درصد و میزان پاسخ کلی 80% تا 90% می باشد.شیمی درمانی قبل از جراحی علاوه برافزودن قابلیت برداشت جراحی، تعداد عقده های لنفی لگنی مثبت را نیز کاهش می دهد و در بعضی مطالعات ظاهراً میزان بقاء دو ساله و سه ساله را بهبود بخشیده است.
اشعه درمانی
اشعه تابی خارجی به لگن معمولاً از طریق یک شتاب دهنده خطی انجام می شود. هدف از درمان خارجی کاهش حجم تومور و کاهش از هم گسیختگی آناتومیک ایجاد شده بوسیله توده های توموری بزرگتر و ایجاد امکان درمان داخل حفره ای بعدی بهینه است.بدنبال درمان خارجی ،درمان اشعه تابی نزدیک با استفاده ازتکنیکهای داخل حفره ای متنوعی،ازجمله Tandem داخل رحمی و کلپوستانهای (Colpostats) واژینال،سیلندرهای واژینال، یا ایمپلنت های سونی بینابینی انجام می شود.
درمان اشعه تابی با عوارض حاد و مزمنی همراه است. پاره شدن رحم ممکن است در زمان وارد کردن داخل حفره ای
منبع اشعه اتفاق افتد و اگر تشخیص داده نشود ممکن است منجر به از دست دادن خون قابل توجه، آسیب اشعه ، و پریتونیت شود. درمان مناسب عبارتست از : برداشتن ایمپلنت و پوشش آنتی بیوتیکی وسیع الطیف در صورتی که علائم عفونت موجود باشد.پروکتوسیگموئیدیت تا 8% بیمارانی که تحت درمان اشعه تابی آن شامل درد شکمی،اسهال و تهوع است یک عامل دارویی ضد اسپاسم،رژیم غذایی با گلوتن و لاکتوز کم،و انمای استروئیدی ممکن است مفید باشند،با این حال موارد شدید ممکن است مفید باشند،با این حال موارد شدید ممکن است نیاز به هیپرالیمانتاسیون و کولستومی انحرافی داشته باشند.سیستیت هموراژیک در حدود 3% از بیمارانی که تحت اشعه درمانی برای کانسرسرویکس قرار می گیرند،دیده می شود.
تنگی واژن شایعترین عارضه مزمن اشعه درمانی برای کانسر سرویکس است و تا 70% موارد دیده می شود.فیستولهای رکتوواژینال و وزیکوواژینال هریک در حدود 15% بیماران کانس سرویکس درمان شده با اشعه اتفاق می افتد. درچنین مواردی نمونه های بیوپسی باید از کناره فیستول برداشته شوند تا احتمال عود کانسر رد شود. منحرف ساختی مدفوع (کولوستومی) یا جریان ادرار (نفروستومی از طریق جلدی) معمولاً برای امکان پذیرساختن ترمیم کافی (3 تا 6 ماه) قبل از ترمیم جراحی مورد نیاز است.
2% از بیماران انسداد روده کوچک را متعاقب اشعه درمانی تجربه می کند که در بیماران با بیماری عروقی یا سابقه جراحی شکمی قبلی شایعتراست.شایعترین محل انسداد روده باریک ایلئوم ترمینال می باشد که بطور نسبی توسط سکوم در موضع اشعه تابی تثبیت شده است. انسداد کامل روده باریک یا موارد سرکش به درمان محافظه کارانه نیاز به مداخله جراحی دارند.
شیمی درمانی
شیمی درمانی در بیماران با متاستازهای خارج لگنی یا بیماران با عود بیماری که کاندیداهای مناسبی برای اشعه درمانی یا جراحی درآوردن احشاء نیستند، اندیکاسیون دارد.سپس پلاتین عاملی است که بیش از همه مورد مطالعه قرار گرفته است و بالاترین میزان پاسخ بالینی مناسب را نشان داده است. پاسخ بالینی کامل در 24% از بیماران مشاهده شده است و 16% دیگر بیماران نیز پاسخ نسبی نشان می دهند. متاسفانه در بشتر موارد پاسخهای به سیس پلاتین کوتاه مدت (3-6ماه) بوده اند. سایر عواملی که حداقل فعالیت نسبی بر علیه کانسرسرویکس نشان می دهند عبارتند از :کاربوپلاتین (پاراپلاتین)،ایفوسفاماید (IFEX)، هیدروکلرید دوکسوروبیسین (آدریامایسین)،ون بلاستین، سولفات ون کریستین (Oncovin)، 5- فلورواوراسیل،متوترکسات،آلترتامین (Hexalen).
شواهد کمی وجود دارند که پیشنهاد کنند که شیمی درمانی مرکب بر درمان تک عاملی سیس پلایتن ارجحیتی در بهبود کلی شانس بقاء بیماران با کانسرسرویکس پیشرفته یا عود کنده داشته باشد.
مطالعه پس از درمان
در میان بیماران با عود کانسر سرویکس، عود در 50درصد بیماران ظرف یک سال و در بیش از هشتاد درصد بیماران ظرف دوسال کشف می شود. معاینه لگنی و بررسی عقده های لنفاوی، شامل عقده های فوق ترقوه ای، باید هر سه ماه برای مدت دوسال و سپس هر شش ماه برای مدت سه سال دیگر انجام شود. بیش از هفتاد درصد بیماران با عود کانسر سرویکس در لگن، نتیجه سلول شناسی غیر طبیعی سرویکس یا واژن خواهند داشت، لذا در زمان هر معاینه روتین ، نمونه های سلول شناسی مناسب باید گرفته شوند. هر توده لگنی قابل لمس باید با CT و صورت اندیکاسیون با سلول شناسی آسپیراسیون سوزن باریک بررسی شود. جهت کشف متاستازهای ریوی باید سالانه یک عکس رادیوگرافی قفسه سینه گرفته شود.
درمان عود کانسرسرویکس
کانسر سرویکس که ظرف 6 ماه اول پس از درمان اولیه کشف شود اغلب کانسر پایدار نامیده می شود، درحالیکه کانسری که بعد از آن تشخیص داده شود بعنوان عود بیماری به آن اشاره می شود. درمان مناسب عود کانسرسرویکس بواسطه محل عود و چگونگی درمان اولیه تعیین می شود، بطورکلی،بیمارانی را که عود بیماری در آنها بدنبال جراحی اولیه بروز می کند، باید برای اشعه درمانی در نظر گرفت.بر عکس،برای بیماران با عود بیماری که در ابتدا اشعه درمانی را دریافت کرده بودند، درمان جراحی باید در نظر گرفته شود. عود متاستاتیک دوردست به هیچیک از روشها به تنهایی
پاسخ نمی دهد و اندیکاسیونی برای شیمی درمانی تسکین دهنده و احتمالاً اشعه درمانی برای کنترل موضعی است.
درمان جراحی عود کانسرسرویکس
تنها بیماران با عود تومور محدود به لگن مرکزی کاندیداهای مداخله جراحی می باشند.هیسترکتومی کلی درمان ناکافی برای عود مرکزی کانسر سرویکس است. بعلاوه هنگامیکه هیستروکتومی رادیکال بدنبال حداکثر دوز اشعه درمانی انجام می شود، 20 تا 50% بیماران تنگی های پیشابراه، فیستولهای ادراری یا دیگر عوارض جدی را تجربه خواهند کرد لذا، تخلیه لگن معمولاً روش جراحی انتخابی برای عود مرکزی کانسر سرویکس است.
جهت رد کردن احتمال متاستازهای خارج لگنی، باید قبل از درمان تخلیه جراحی، یک بررسی کامل بعمل آورد. تریاد بالینی ادم یکطرفه پا، درد سیاتیک و انسداد حالب از گسترش تومور به دیواره جانبی لگن خبر می دهد و کنتراندیکاسیونی برای جراحی است، در اغلب سری های مطالعاتی، تقریباً 25% بیماران با عود کانسر سرویکس،کاندیداهای رضایتبخشی برای درمان تخلیه جراحی در نظر گرفته می شوند.
تخلیه قدامی برای درمان عود کانسر سرویکس محدود به سرویکس،واژن قدامی و / یا مثانه اندیکاسیون دارد.این روش سیستکتومی رادیکال را با هیسترکتومی رادیکال و واژنکتومی در هم می آمیزد. تخلیه خلفی برش پرینئال شکمی رکتوم را با هیسترکتومی رادیکال واژنکتومی ترکیب می کند وبرای ضایعات محدود به فورنیکس خلفی و دیواره بین واژن و رکتوم اندیکاسیون داردو تخلیه کلی لگن در اغلب موارد برای عود کانسر سرویکس ضرورت می یابد.این روش شامل بریدن و بیرون آوردن مثانه، رحم، رکتوم و واژن،همه با هم،می شود(شکل22).
با استفاده از وسایل اتصال جراحی موجود، آناستوموز مجدد پایین رکتوم را می تواند در حدود 70% موارد انجام داد. بازسازی سیستم ادراری با استفاده ازیک مجرای روده ای ادراری یا یکی از تکنیک های منحرف سازی ادراری (کیسه میامی، کیسه ایندیانا) انجام می شود. بوسیله تکنیک های گوناگون و با استفاده از زباله های پیوندی جلدی عضلانی (مثلاً بولبوکاورنوس، گراسیلیس، عضله رکتوس متقاطع شکمی) می توان یک واژن جدید ایجاد کرد.
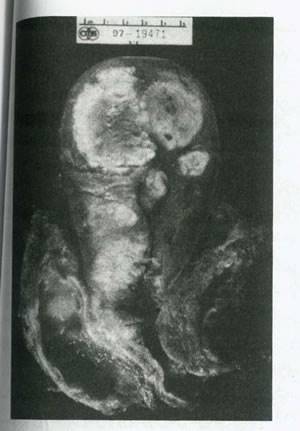
شکل 22.تخلیه ی کلی لگن که برای درمان عود کانسر سرویکس انجام می شود،شامل برداشتن دسته جمعی مثانه واژن ،رحم و رکتوم است.در این نمونه ،عود کانسر سرویکس ،سرویکس را درگیر کرده است(لیومیومای رحم فوندوس رحم را اشغال کرده است).
با وجود تکنیک های نوین جراحی و حمایت بوسیله بخش مراقبت های ویژه، مرگ و میر عمل جراحی در سری های مطالعاتی اخیر از 0/07تجاوز نمی کند. با انتخاب مناسب بیماران و قضاوت صحیح جراحی،میزان بقاء 5سال پس از تخلیه لگن بین 45 تا 61% است.
آدنوکارسینوم
آدنوکارسینوم سرویکس مسئول حدود 10 تا 0/015 تمامی نئوپلاسم های مهاجم سرویکس است. همانند SCC اندازه تومور، عمق تهاجم و درجه بافت شناسی تومور بعنوان پیش گویی کننده های متاستازهای عقده ای لنفاوی لگنی و شانس بقاء کلی شناسایی شده اند. اگر چه آدونوکارسینوم سرویکس با پیش آگهی بدتر از SCC هم درجه گزارش شده است، این اختلاف،حداقل تا حدودی به علت تمایل آدنوکارسینوم به رشد آندوفیتیک و بوجود آوردن یک تومور حجیم قبل از کشف بالینی است. وقتیکه آدنوکارسیوم
سرویکس و SCC به نسبت سن بیمار، درجه بالینی، حجم تومور، وروش درمان مقایسه شوند، نتایج بقاء تفاوت چشمگیری ندارند.
کارسینوم سلول کوچک
کارسینوم سلول کوچک سرویکس مشابه تومور«نوروآندوکرین» سلول کوچک ریه و سایر محلهای آناتومیک است. این تومورها از لحاظ بالینی مهاجم اند وتمایل زیادی به متاستاز دادن به نواحی موضعی و دور نشان می دهند. بیماری در زمان تظاهر اغلب وسیعاًانتشار یافته است،استخوان، مغز و کبد شایعترین محل ها می باشند.به علت استعداد ذاتی متاستاتیک زیاد کارسینوم سلول کوچک،درمان موضعی به تنهایی (جراحی و یا اشعه درمانی) بندرت منجر به بقاء طویل المدت بیمار می شود. شیمی درمانی با چند دارو، همراه با درمان اشعه درمانی از خارج بدن و داخل حفره رحمی روش درمانی است که در حال حاضر تحت مطالعه می باشد. دو رژیم دارویی شیمی درمانی که شایعتر از همه مورد استفاده قرار می گیرند عبارتند از ون کریستین، دوکسوروبی سین (آدریامایسین) و سیلکوفسفامید (VAC) و اتوپوزیدوسیس پلاتین (EP).
کارسینوم انتهای سرویکس
تاریخچه طبیعی و طرح های گسترش کارسینوم انتهای سرویکس مشابه کارسینوم خود رحم هستند.ارزیابی تشخیصی، درجه بندی بالینی، و اصول درجه بندی نیز تفاوتی با هم ندارند. در بیماران کاندید جراحی مناسب، بیماری در مراحل اولیه را می توان با تراکلکتمی ساده یا رادیکال با یا بدون لفنادنکتومی،بسته به حجم تومور، درمان کرد. بیماری در مراحل پیشرفته با اشعه درمانی معالجه می شود. با این حال، فقدان یک حفره رحمی می تواند قرار دادن منشاء تابش اشعه داخل حرفه ای را مشکل یا غیر ممکن سازد. در این مورد، می توان از اجسام تخم مرغی واژینال به تنهایی یا یک تکنیک ایمپلنت سوزنی بین بافتی همراه با اشعه درمانی از خارج استفاده کرد.
کانسر سرویکس تصادفی یافت شده در حین هیسترکتومی ساده
کانسر مهاجم سرویکس ممکن است بصورت تصادفی در نمونه گرفته شده جراحی پس ازانجام هیسترکتومی کشف شود. برای بیماری پیشرفته تر از درجه IA1 (بدون درگیری لنفی عروقی)، هیسترکتومی ساده درمان کافی نمی باشد، چرا که پارامتر،کاف واژنی و عقده های لنفاوی لگنی ممکن است پناهگاه تومور باقیمانده باشند. درمان اضافی بواسطه حجم بیماری و وضعیت حاشیه های جراحی برای برش تعیین می شود.
جراحی رادیکال برای کانسر مهاجم سرویکس متعاقب هیسترکتومی ساده معمولاً شامل پارامترکتومی رادیکال، برش لیگامانهای کاردینال، بریدن و در آوردن انتهای واژن و لنفادنکتومی لگنی می شود. اگر چه ممکن است از لحاظ تکنیکی انجام رزکسیون رادیکال کافی مشکل باشد، جراحی مجدد باید در وضعیت های انتخابی بالینی،خصوصاً برای بیماران جوان که حفظ تخمدانها در آنها مطلوب است، درنظر گرفته شود. استفاده از اشعه درمانی کمکی بعد از عمل توسط یافته های جراحی و پاتولوژیک تعیین می شود.
کارسینوم سرویکس در حاشیه های برش جراحی پس از هیسترکتومی ساده یا وجود تومور باقیمانده بزرگ اندیکاسیون های مطلق جهت اشعه درمانی هستند. بیماران با چنین یافته هایی پیش آگهی بسیار نامطلوبتری نسبت به بیماران بدون تومور باقیمانده و بیماران با بیماری برابر که بطور مناسبی درجه بندی و با اشعه درمانی تنها درمان شده اند،دارند.اشعه درمانی همچنین برای بیماران مسن تر یا بیمارانی که کاندیداهای خوبی برای جراحی نیستند، مناسب است. میزان بقاء پنج ساله برای بیماران با بیماری میکروسکوپی 95 تا 100% است، در حالیکه 82 تا 84% بیماران با بیماری ماکروسکوپیک و حاشیه های جراحی منفی 5 سال زنده می مانند. اگر حاشیه های جراحی منفی 5 سال زنده می مانند. اگر حاشیه های جراحی محل برش بطور میکروسکوپی درگیر باشند میزان بقاء 5 ساله در محدوده 38 تا 87% است. میزان بقاء برای بیماران با تومور باقیمانده بزرگ به 20 تا 47% سقوط می کند.
کولپوسکوپی
کولپوسکوپی در سال 1925 توسط Hinselman ابداع شد و اگر چه در کشورهای آلمانی زبان و در آمریکای جنوبی وسیعاً مورد استفاده قرار می گرفت، درکشورهای انگلیسی زبان، به استثنای استرالیا توجه نسبتاً کمی بخود جلب کرد. علت تاخیر در پذیرفتن کولپوسکوپی در انگلستان و ایالات
متحده بیشتر واژه شناسی شدیداً تکنیکی و مشکل هینزلمن بود که بیشتر آن از تاثیرات بصری ریشه می گرفت که ضرورتاً ارتباطی با فرایند های هیستوپاتولوژیک زمینه ای نداشتند.ظهور سلول شناسی تشخیصی با ورقه های سازی نیز معرفی کولپوسکوپی را در کشورهای انگلیسی زبان به تأخیرانداخت. یاد گرفتن اینکه چگونه باید یک نمونه کافی از سرویکس برداشت بسیار ساده تر از یاد گرفتن نحوه استفاده از کولپوسکوپ است. آموزش کولپوسکوپی وقت گیراست و بدون آموزش کافی،بدست آوردن نتایج خوب غیرممکن است.
کولپوسکوپی و سلول شناسی برای مدتها بعنوان روشهای رقیب در کشف زودرس کانسر درنظرگرفته می شوند.با وجود این هریک ازاین روشها محدودیت ها و نقاط قوت خاص خود را در کشف کانسر دارد، و این دو روش یکدیگر را کامل می کنند. سلول شناسی روشی آزمایشگاهی و کولپوسکوپی یک روش بالینی اکتشاف است. هریک ازآنها با جنبه متفاوتی از نئوپلازی سروکار دارند. سلول شناسی تغییرات مورفولوژیک را در سلولهای ورقه ورقه شده بررسی می کند و کولپوسکوپی تغییرات درشبکه عروقی انتهایی سرویکس بررسی می کند که منعکس کننده ی تغییرات بیوشیمیایی و متابولیک دربافت است.

تکنیک
کولپوسکوپ اساساً یک میکروسکوپ سه بعدی است که با آن می تواند سرویکس را که 6 تا 40 برابر بزرگنمایی شده در نور روشن دید (شکل23). تکنیک معاینه سریع است و تنها کمی بیش از مشاهده سرویکس با چشم غیر مسلح وقت نیاز دارد. پس از اینکه نمونه برای مطالعه سلولی گرفته شد، مواد مخاطی بدقت با استفاده از یک سواب از روی سرویکس برداشته می شود. سپس کولپوسکوپ بر روی سرویکس میزان می شود .در معاینه کولپوسکوپی روتین از بزرگنمایی 16 برابر استفاده می شود.سپس سرویکس با اسید استیک 3 تا 5% خیسانده می شود تا نمای نواحی غیر طبیعی را مشخص تر کند. اپی تلیوم متاپلاستیک، دیسپلاستیک، یا CIS بواسطه نمای سفیدش توصیف می شود.با قراردادن یک فیلتر سبز،کنتراست بهینه عروقی بدست می آید. تاثیراسید استیک تنها برای چند دقیقه طول می کشد،ولی اگر معاینه طولانی تر مورد نظرباشد سرویکس را می تواند مجدداً با اسید استیک خیساند.
یافته های کولپوسکوپی
واژه شناسی و طبقه بندی ضایعات
در سال 1978 در طی سومین کنگره جهانی برای پاتولوژی سرویکس و کولپوسکوپی درارلاندو،فلوریدا، یک واژه شناسی کولپوسکوپی به چهار دسته تقسیم می شوند: طبیعی، غیر طبیعی ، غیر رضایت بخش و سایر موارد.
یافته های کولپوسکوپی طبیعی
اپی تلیوم سنگفرشی طبیعی، اپی تلیوم صاف، صورتی و بدون طرح است که ذاتاً برروی سرویکس و واژن قرار دارد هیچ بقایایی از اپی تلیوم استوانه ای، مانند اپی تلیوم ترشح کننده مخاط، دهانه شکاف یا کیست های نابوتین در آن شناسایی نمی شود (شکل24).
اپی تلیوم استوانه ای یک لایه منفرد سلول های اپی تلیومی طویل و تولید کننده مخاط است که از اپی تلیوم سنگفرشی اصلی با اپی تلیوم متاپلاستیک به آندوسرویکس گسترش می یابد. ناحیه پوشانده شده با اپی تلیوم استوانه ای سطح بی نظمی با پاپیلاهای استرومایی طویل و شکافهای عمیق دارد. پس از استعمال اسید استیک، این اپی تلیوم یک ساختمان انگور شکل تیپیک را آشکار می سازد. اپی تلیوم استوانه ممکن است در قسمت مهبلی رحم (Portio ) موجود باشد و یا به واژن گسترش یافته باشد.
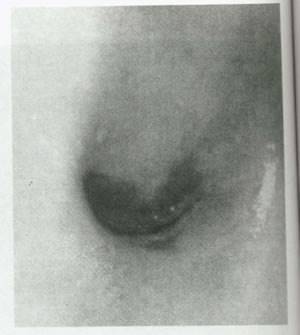
شکل 24.در اپی تلیوم سنگفرشی طبیعی شبکه ی عنکبوتی شکل سطحی مویرگی به زحمت قابل رویت است.(بزرگنمائی 16 برابر)
منطقه تغییرشکل ناحیه ای بین اپی تلیوم سنگفرشی اصلی و اپی تلیوم استوانه ای است که درآن اپی تلیوم متاپلاستیک در درجات مختلف بلوغ سلولی شناسایی می شود.اجزاء منطقه تغییر شکل طبیعی شامل جزایر اپی تلیوم استوانه ای هستند که با اپی تلیوم متاپلاستیک،دهانه های غدد و کیست های نابوتین احاطه شده اند،در منطقه تغییر شکل طبیعی هیچ یافته کولپوسکوپی که پیشنهاد کننده نئوپلازی سرویکس باشد وجود ندارد (شکل 25).
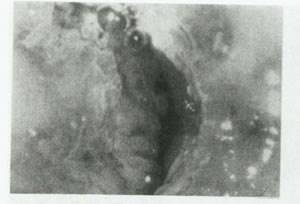
شکل25.در منطقه تغییر شکل طبیعی ،جزایر متاپلازی سنگفرشی و زبانه های اپی تلیوم استوانه ای (ساختمان های انگور شکل)در سمت راست دهانه ی خارجی سرویکس بیمار دیده می شوند.
یافته های کولپوسکوپی غیرطبیعی
منطقه تغییرشکل آتیپیک حاوی یک یا بیشتر از یافته هایی است که پیشنهاد کننده نئوپلازی سرویکس هستند:اپی تلیوم سفید استواستیک،نقطه گذاری،طرحی عروقی موزایئک، هیپرکراتوز، و عروق خونی غیر طبیعی .
* اپی تلیوم سفید استواستیک یک ضایعه کولپوسکوپی غیرطبیعی موضعی است که پس از استعمال اسید استیک دیده می شود. این پدیده گذرا در ناحیه افزایش تراکم هسته ای دیده می شود.
* نقطه گذاری یک ضایعه کولپوسکوپی غیر طبیعی موضعی با طرح عروقی نقطه نقطه است که بوسیله قوسهای مویرگی در پاپیلاهای استرومایی که از انتها دیده می شوند،ایجاد می شود.حدود تغییرات عروقی در مقابل اپی تلیوم طبیعی دقیقاً مشخص است (شکل26).
* درضایعه کولپوسکوپی غیر طبیعی موضعی با طرح موزاییک، حوزه های موزاییک توسط حاشیه های قرمزی مجزا می شوند که بوسیله قوسهای مویرگی ایجاد شده اند که در نمای مقطعی اپی تلیوم دیده می شوند (شکل 27).
* هیپرکراتوزیک طرح کولپوسکوپی موضعی است که در آن هیپرکراتوزیاپاراکراتوز به شکل یک پلاک سفید برجسته آشکار می شود. این پلاک سفید قبل از استعمال اسید استیک شناسایی می شود.بعضی موارد هیپرکراتوز می توانند در خارج از منطقه تغییرشکل شناسایی شوند.
* عروق خونی غیر طبیعی یک طرح کولپوسکوپی غیر طبیعی موضعی را تشکیل می دهند که درآن عروق خونی نه به شکل نقطه گذاری،موزاییک یا عروق با انشعابات ظریف،بلکه به صورت عروق بی نظمی با مسیرهای منقطع ظاهر می شوند که به شکل کاما،مویرگهای پیچیده یا اشکال اسپاگتی شکل که به موزات سطح امتداد دارند،دیده می شوند.
یک نوع دیگریافته های غیر طبیعی کانسر مهاجم آشکار در کولپوسکوپی است که در معاینه بالینی آشکار نمی شود (شکل 29).
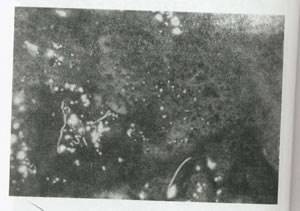
شکل 26.
الف:نقطه گذاری روی لب قدامی سرویکس با مقداری اپی تلیوم سفید مخلوط شده است.یک نمونه بیوپسی از این ناحیه دیسپلازی شدید نشان داد .ب:استفاده از یک فیلتر سبز روی کولپوسکوپ ظاهر شدن نقطه گذاری را افزایش می دهد.
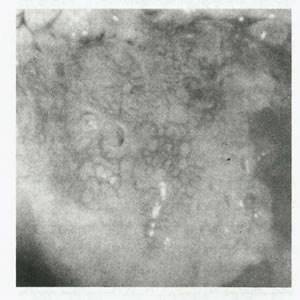
شکل 27.یک طرح موزاییک در درون اپی تلیوم سفید دیده می شود.یک بیوپسی از این ناحیه کارسینوم درجارا نشان داد.
یافته های کولپوسکوپی غیر رضایت بخش
عنوان کولپوسکوپی غیر رضایت بخش هنگامی به کار گرفته می شود که نتوان حدود محل اتصال سنگفرشی استوانه ای را تعیین کرد و یا گسترش اندوسرویکال یک ضایعه مشاهده شده را نتوان رویت کرد.
سایر یافته های کولپوسکوپی
چندین یافته کولپوسکوپی دیگر وجود دارند. درالتهاب واژن و سرویکس، یک طرح منتشر کولپوسکوپی پرخونی وجود دارد که در آن عروق خونی دریک طرح نقطه نقطه شبیه به طرح عروقی در نقطه گذاری ظاهر می شوند(شکل 30). درفرسایش واقعی، معاینه کولپوسکوپی یک ناحیه برهنه شده از اپی تلیوم را آشکار می سازد. این وضعیت معمولاً بواسطه تروما ایجاد می شود. اپی تلیوم اتروفیک یک اپی تلیوم سنگفرشی محروم از استروژن است که در آن طرح عروقی بعلت نازک بودن نسبی اپی تلیوم سنگفرشی پوشاننده سریعاً شناسایی می شود. کوندیلوما و پاپیلوما ضایعات اگزوفیتیک هستند که ممکن است درون یا بیرون منطقه تغییر شکل باشند.
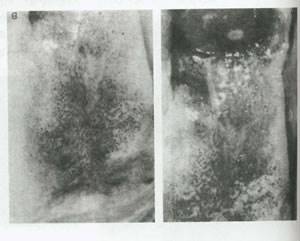
شکل 28.عروق آتیپیک .عروق انتهایی از لحاظ اندازه ،شکل و نحوه ی قرارگیری بی نظمند .نمونه های بیوپسی کارسینوم مهاجم را آشکار ساخته است.
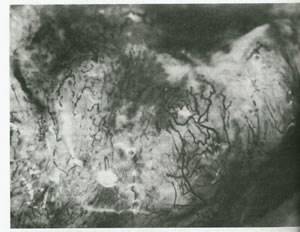
شکل 29.کانسر مهاجم واقعی مشکوک .شاخه شدن آتیپیک و عروق شبکه با کانسر واقعی مهاجم مطابقت دارند.بیوپسی تشخیص را قطعی خواهد ساخت.
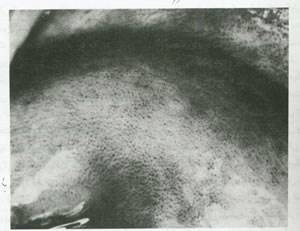
شکل30.اپی تلیوم اسکواموس اصلی با تغییرات التهابی .عروق انتهایی در عفونت تریکومونایی ممکن است تصویر کولپوسکوپیک منقوط را نشان دهد اما مویرگ ها به صورت منتشر روی اکتوسرویکس و دیواره ی واژن دیده می شوند.
ارتباط بین یافته های کولپوسکوپی و بافت شناسی
جدول 8 واژه شناسی کولپوسکوپی را با نمای کولپوسکوپی و تغییرات بافت شناسی مورد انتظار مرتبط می سازد. یافته های کولپوسکوپی طبیعی مربوط به اپی تلیوم اصلی طبیعی سرویکس (یعنی سنگفرشی یا استوانه ای) یا اپی تلیوم سنگفرشی متاپلاستیک می باشند.دربیماران با یافته های کولپوسکوپی طبیعی که در آنها محل اتصال سنگفرشی استوانه ای کاملاً قابل رویت است، نئوپلازی سرویکس نباید در بافت وجود داشته باشد.
شایعترین یافته های کولپوسکوپی غیر طبیعی عبارتند از اپی تلیوم سفید استواستیک،نقطه گذاری و یک طرح موزاییک. چون پاتوژنز این طرح ها مشابه است، ترکیب این یافته ها شایع است. مشابه بافت شناسی این طرح ها از تغییرات دیسپلاستیک حداقل تا CIS می باشند. برای پیشگویی تغییرات هیستوپاتولوژیک دریک بیوپسی راهنمایی شده،اهمیت ندارد که ضایعه مشاهده شده در کولپوسکوپی بصورت اپی تلیوم سفید، نقطه گذاری یا طرح موزاییک بنظر برسد. این تغییرات هیستوپاتولوژیک را می توان با رجوع به خصوصیات سادگی قابل مشاهده کولپوسکی پیشگویی کرد: طرح عروقی، فاصله بین مویرگی، طرح سطحی، رنگ و وضوح حدود.
طرح عروقی یکی از مهمترین خصوصیات تشیخص است. تغییرات در طرح عروقی بدقت با درجه تغییرات بافت شناسی مطابقت دارند. در طی مرحله اول کارسینوژنز، مورفولوژی بافت تغییر نکرده است،ولی عروق خونی به این تغییرات در متابولیسم بافتی و بیوشیمی سلولی واکنش نشان داده و تغییرات عروقی اولین اختلال مورفولوژیک را در ظهور نئوپلازی سرویکس تشکیل می دهند.برای توصیف مفصل طرح های عروقی مختلف و اهمیت تشخیصی آنها، خواننده باید به مقالات کولپوسکوپی مراجعه کند.
فاصله بین مویرگی به مقداربافت سرویکس که عروق خونی را از هم جدا می سازد اطلاق شود. درحین یک معاینه کولپوسکوپی،فاصله بین مویرگی را در یک ضایعه غیر طبیعی کولپوسکوپی می توان با مقایسه با مویرگهای اپی تلیوم طبیعی مجاور تخمین زد.درنئوپلازی سرویکس، فاصله بین مویرگی به موازات پیشرفت درجه بیماری افزایش می یابد.
کولپوسکوپ یک بزرگنمایی سه بعدی فراهم می کند که مطالعه نقشه سطحی را بسیار تسهیل می کند و می تواند آن را به عنوان صاف، ناهموار،دانه دانه، پاپیلوماتوز، یاندولر توصیف کند. اپی تلیوم سنگفرشی طبیعی یا دیسپلازی حداقل سطح صاف دارد، CIS و کارسینوم مهاجم در مراحل اولیه سطح ناهموار مختصری برجسته دارند.
ضایعات کولپوسکوپی زمینه رنگ متفاوتی دارند، که از سفید تا قرمز تیره متغیر است. تفاوت بین رنگ سطح سرویکس قبل و بعد از استعمال اسید استیک، تغییررنگ بارزی از قرمز تیره به سفید وجود داشته باشد، می توان انتظار یک ضایعه بافت شناسی شدید را داشت. مهم است که سرویکس را قبل و بعد از استعمال اسید استیک با کولپوسکوپی معاینه کرد.
یک خصیصه مهم ضایعه غیر طبیعی کولپوسکوپی واضح بدون حدود بین ضایعه و بافت طبیعی مجاور است. حد مرز بین اپی تلیوم سنگفرشی طبیعی و تغییرات التهابی یا دیسپلازی حداقل گسترده و نامنظم است.دیسپلازی شدید یا CIS معمولاً یک ضایعه با حدود واضح ایجاد می کند که آن را بوضوح از اپی تلیوم طبیعی مجاور متمایز می کند.
ارزش اصلی کولپوسکوپی در ارزیابی بیمارانی که مطالعات سلول شناسی شان غیرطبیعی اند و در معرض نئوپلازی بارز سرویکس قرار دارند،کولپوسکوپی این امکان را فراهم می سازد که ضایعات مهاجم از غیر مهاجم و آتیپی التهابی از نئوپلازی دقیق است.دربیمارانی که سلول های غیرطبیعی در سلول شناسی دارند، کولپوسکوپی می تواند بلافاصله بین تغییرات التهابی و نئوپلاستیک افتراق دهد. محدودیت کولپوسکوپی در ناتوانی آن برای کشف یک ضایعه عمیق در کانال آندوسریکال است که نتایج کولپوسکوپی در این مورد،بعلت قابل رویت نبودن محل اتصال سنگفرشی استوانه ای،ممکن است غیر رضایتبخش باشند. گامهای تشخیصی بیشتری در این مورد ضرورت دارند. کثرت وقوع یافته های کولپوسکپی غیر رضایتبخش در زنان قبل از یائسگی 12 تا 15% است.پس از یائسگی، کثرت وقوع کولپوسکوپی غیر رضایتبخش بطور چشمگیری افزایش
می یابد،بنحوی که ارزش کولپوسکوپی در بررسی سرویکس زنان پس از یائسگی محدودتراست. با وجود این، دربیمارانی که محل اتصال سنگفرشی استوانه ای شان کاملاً قابل رویت است، میزان منفی کاذب در کولپوسکوپی اندک می باشد.
کولپوسکوپی همچون هر روش تشخیصی دیگر محدودیت هایی دارد که باید کاملاً شناخته شوند.هرچه بر اهمیت آموزش و تجربه کافی تاکید شود،زیاده از حد نخواهد بود. بی تجربگی می تواند منجر به اشتباهات جدی در تشخیص و درمان کانسر سرویکس شود که ممکن است موجب بی اعتباری اساسی کولپوسکوپی گردد. محدودیت کولپوسکوپی در تشخیص ضایعات در کانال آندوسرویکس باید کاملاً درک شود،و هنگامی که محل اتصال سنگفرشی استوانه ای کاملاً قابل رویت نباشد.روشهای دیگر بررسی (مثلاً ECC، مخروط برداری) باید مورد استفاده قرار گیرد. کولپوسکوپی هنگامیکه آگاهانه و بادرک کامل تمام جزئیات مورفولوژی انجام گیرد،ابزار تشخیص مهمی برای طبابت بالینی وتحقیقات است.
جدول 8:ارتباط بین یافته های کولپوسکوپی و بافت شناسی
|
قرینه ی بافت شناسی
|
نمای کولپوسکوپی
|
واژه کولپوسکوپی
|
|
اپی تلیوم سنگفرشی
|
صاف،صورتی ،با طرح نامعین،بدون تغییر پس از استعمال اسید استیک
|
اپی تلیوم سنگفرشی طبیعی
|
|
اپی تلیوم استوانه ای
|
ساختمان های انگور شکل پس از استعمال اسید استیک
|
اپی تلیوم استوانه ای
|
|
اپی تلیوم سنگفرشی متاپلاستیک
|
زباله های متاپلازی سنگفرشی،دهانه ی غدد،کیستهای نابوتین
|
منطقه تغییر شکل
|
|
دیسپلازی حداقل تا کارسینوم درجا
|
ضایعه ی سفید با حدود واضح که تنها پس از استعمال اسید استیک قابل رویت است،عروق قابل رویت نیستند.
|
اپی تلیوم سفید
|
|
دیسپلازی حداقل تا کارسینوم درجا
|
ضایعه ی با حدود واضح،نقطه نقطه ی قرمز،اپی تلیوم پس از استعمال اسید استیک سفید تر می شود.
|
نقطه گذاری
|
|
دیسپلازی حداقل تا کارسینوم درجا
|
ضایعه ی با حدود واضح ،طرح موزاییک ،اپی تلیوم پس از استعمال اسید استیک سفید تر می شود.
|
موزاییک
|
|
معمولاً هیپرکراتوز یا پاراکراتوز ،ندرتاً کارسینوم درجا یا کارسینوم مهاجم
|
لکه سفید ،سطح زبر ،قبل از استعمال اسید استیک قابل رویت است.
|
هیپرکراتوز
|
|
کارسینوم درجا تا کارسینوم مهاجم
|
عروق افقی که به موازات سطح امتداد دارند،تنگی یا گشادی عروق ،انشعابات آتیپیک ،مسیر مارپیچ.
|
عروق آتیپیک
|
منبع:مامایی و بیماریهای زنان دنفورث(جلد دوم)
/ج